.(12分)某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,某同学设计如下试验:
(1)取样品 ag ,称取时使用的仪器名称为 。
(2)将样品溶于足量的稀盐酸中,过滤,滤渣中含有 ,在溶解过滤时使用的玻璃仪
器有 。
(3)往滤液中加入过量的NaOH溶液、过滤,写出该步操作中有关的离子方程式 。
(4)在第( 3 )步的滤液中通入足量CO2,过滤。有关反应的离子方程式是 。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次后,烘干并灼烧至质量不再减轻为止,冷却后称量,质量为bg,则原样品中铝的质量分数是 。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏 (填“高”、“低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏 ;若滤渣燃烧不充分,则实验结果偏 。
(1)托盘天平 (2)硅、铜;烧杯、漏斗、玻璃棒
(3) Al3+ + 4OH- = [Al(OH)4]-、Mg2+ + 2OH- = Mg(OH)2↓
(4) [Al(OH)4]-+ CO2 = Al(OH)3↓+ HCO3- (5) 9b/17a (6) 低 ;高 ;高
(1)称量固体药品使用托盘天平。
(2)铜、硅和盐酸不反应,所以滤渣是铜和硅。溶解过滤时使用的玻璃仪器有烧杯、漏斗、玻璃棒。
(3)加入强酸生成氢氧化镁和氢氧化铝沉淀,但氢氧化铝是两性氢氧化物,能溶于强碱中。有关的方程式为Al3+ + 4OH- = [Al(OH)4]-、Mg2+ + 2OH- = Mg(OH)2↓。
(4)滤液中含有偏铝酸盐,通入CO2生成氢氧化铝沉淀,方程式为[Al(OH)4]-+ CO2 = Al(OH)3↓+ HCO3-。
(5)沉淀是氢氧化铝,灼烧得到氧化铝,所以铝放热质量分数为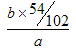 =9b/17a。
=9b/17a。
(6)若步骤(3)中加入氢氧化钠的量不足,则滤液中偏铝酸盐的量就偏低,最后结果偏低。若步骤(5)中滤渣没有洗涤,则实验结果偏,则氢氧化铝的质量偏大,结果偏高。若滤渣燃烧不充分,则氧化铝就偏高,结果偏高。
