.(12分)在实验室中用二氧化锰跟浓盐酸反应制备干燥且较纯净的氯气。进行此实验,所用仪器如下图:
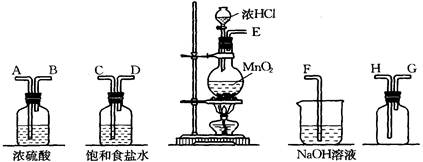
(1)连接上述仪器的正确顺序是(填各接口处的字母):
接 ,_____接 ,_____接 , 接 。
(2)在装置中:
①饱和食盐水的作用是 ,
②浓硫酸的作用是 。
(3)写出下列化学反应的化学方程式:
①气体发生装置中进行的反应: ;
②尾气吸收装置中进行的反应: 。
(4)MnO2是______色的粉末状固体,在该实验中MnO2所起得作用是____________
(5)若实验操作正确,在集气瓶内若放一块干燥的有色布条,在实验进行的过程中,有色布条能否褪色?(填“能”或“不能”)________.
(共12分)
(1)E 接 C , D接 A , B接 H ,G 接 F。(2分)
(2)① 除去氯气中的HCl气体,(1分)
②除去氯气中的水蒸气,干燥氯气 。(1分)
(3)①:4HCl(浓)+MnO2 MnCl2 +Cl2↑ +2H2O;(2分)
MnCl2 +Cl2↑ +2H2O;(2分)
②:Cl2 + 2NaOH =" NaCl" + NaClO + H2O(2分)
(4)黑,(1分)氧化剂(或类似的意思)(1分)
(5)不能(2分)
考查氯气的制取、除杂、干燥及尾气吸收:其中一般用饱和食盐水来吸收氯化氢,浓硫酸来吸水,用碱液来吸收尾气
在实验原理中,MnO2是氧化剂,将盐酸中的氯元素氧化为氯气
干燥、除杂、集气时气体一般是长管进、短管出;
氯气本身并没有漂白性,只有当与水反应生成次氯酸时才具有漂白性,故经干燥后、在集气瓶中收集的氯气没有漂白性
