(9分)(2013•安庆一模)小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂.于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣.
【提出问题】氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列几组实验.
| 序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
| ① | 2.0g | 330℃ | 100mL | t1 | |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | t2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | t3 |
| ④ | 2.0g | MnO2 _________ g | 380℃ | 100mL | t4 |
(2)你认为小雨设计实验③和实验②对比的目的是 _________ .
(3)实验④中MnO2的质量为 _________ g,若t3>t4,则化学反应快慢与温度的关系是 _________ .
(4)写出实验④所涉及的化学方程式 _________ .
(1)> 质量 化学性质
(2)探究氧化铜是否比二氧化锰的催化效果更好
(3)0.5 温度越高,反应速率越快
(4)2KClO3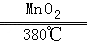 2KCl+3O2↑
2KCl+3O2↑
题目分析:(1)如果氧化铜能加快氯酸钾的分解速率,那么所用的反应时间就会减少,即实验①比实验②所用时间多,故t1>t2,催化剂:在化学反应中能改变其他物质的反应速率(加快或变慢),但本身的化学性质和质量在反应前后没有发生变化的物质,特点:两不变(质量、化学性质)、一改变(反应速率),所以若要确定氧化铜是此反应的催化剂,还需探究反应前后氧化铜的质量和化学性质不变
(2)从图中数据看,KClO3的质量、温度、氧气的体积均相同,因此实验③和实验②对比的目的是探究氧化铜是否比二氧化锰的催化效果更好
(3)从图中数据看,实验④中控制MnO2的质量为0.5g,若t3>t4,则化学反应快慢与温度的关系是温度越高,反应速率越快
(4)氯酸钾在二氧化锰做催化剂、380℃时分解生成氯化钾和氧气,反应的化学方程式是:2KClO3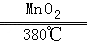 2KCl+3O2↑.
2KCl+3O2↑.
