A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA的单质能跟足量的盐酸反应,在标准状况下可置换出22.4L的H2,这时A转变为与氖原子具有相同电子层结构的离子.试回答:
(1)写出A和C组成的化合物的电子式______;
(2)B的离子结构示意图是______,与B的离子具有相同电子数的分子中,有一种分子可与盐酸化合生成一种盐,该盐的电子式是______;
(3)写出C元素的单质和甲烷发生一元取代反应的化学方程式______;
(4)写出A最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式:______.
A、B、C三种元素的原子具有相同的电子层数,1molA的单质能跟足量的盐酸反应,在标准状况下可置换出22.4L的H2,A为金属,令A反应后化合价为x,则根据电子转移守恒,1x=2,所以x=2,即A反应后为+2价,这时A转变为与氖原子具有相同电子层结构的离子,则A为镁元素.而B的核电荷数比A大1,则B为铝元素;C原子的电子总数比B原子的电子总数多4,则C为氯元素.
(1)A为镁元素,C为氯元素,二者形成氯化镁,是离子化合物,有镁离子与氯原子构成,电子式为
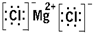
.
故答案为:
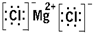
.
(2)B的离子是铝离子,质子数为13,核外电子数为10,有2个电子层,最外层有8个电子,结构示意图是
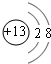
;与铝离子具有相同电子数的分子中,有一种分子可与盐酸化合生成一种盐,该盐是氯化铵,氯化铵是离子化合物有铵根离子与氯离子构成,电子式是
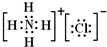
.
故答案为:

;
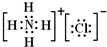
.
(3)氯气和甲烷发生一元取代反应生成一氯甲烷和氯化氢,反应化学方程式CH4+Cl2
CH3Cl+HCl.光照
故答案为:CH4+Cl2
CH3Cl+HCl.光照
(4)A最高价氧化物的水化物为氢氧化镁,C最高价氧化物的水化物为高氯酸,二者反应的离子方程式:
Mg(OH)2+2H+=Mg2++2H2O.
故答案为:Mg(OH)2+2H+=Mg2++2H2O.
