(13分)氯气是一种重要的工业原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
(2)资料显示:Ca(ClO)2 +CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
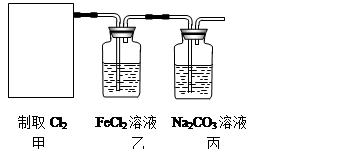
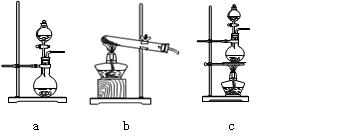
①在该实验中,甲部分的装置是 (填字母)。
②乙装置中FeCl2溶液与Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是 。
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是 。
④该实验存在明显的缺陷,改进的方法是 。
(3)为测定漂白粉中Ca(ClO)2的质量分数,该小组将2.0 g漂白粉配制成250 mL溶液,取出25 mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入0.1 mol/L Na2S2O3溶液:2Na2S2O3+I2 ="==" Na2S4O6+2NaI,共消耗20 mL Na2S2O3,则漂白粉中Ca(ClO)2的质量分数为 。
(1)MnO2 + 4HCl(浓)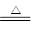 MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(2)① c (1分) ②2Fe2++Cl2 ="==" 2Fe3++2Cl-
取少量反应后的溶液置于洁净的试管中,向其中滴加KSCN溶液,若产生红色溶液,证明生成了Fe3+ ,即FeCl2与Cl2发生了氧化还原反应(合理即得分)
③Cl2+2Na2CO3+H2O ="==" NaCl+NaClO+2NaHCO3
④在丙装置后连接一个盛有氢氧化钠溶液的洗气瓶(合理即得分)
(3)35.75%
(1)方程式为MnO2 + 4HCl(浓)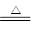 MnCl2 + Cl2↑+ 2H2O。
MnCl2 + Cl2↑+ 2H2O。
(2)①根据反应原理可知,反应需要加热,硫酸是溶液,所以应该选择c装置。
②氯气具有氧化性,能把氯化亚铁氧化生成氯化铁,方程式为2Fe2++Cl2 ="==" 2Fe3++2Cl-。由于生成物是氯化铁,所以要证明FeCl2与Cl2发生了氧化还原反应,可以通过检验铁离子来证明。即取少量反应后的溶液置于洁净的试管中,向其中滴加KSCN溶液,若产生红色溶液,证明生成了Fe3+ ,即FeCl2与Cl2发生了氧化还原反应。
③由于碳酸的酸性强于次氯酸,所以反应中不可能生成CO2,因此方程式为Cl2+2Na2CO3+H2O ="==" NaCl+NaClO+2NaHCO3。
④由于氯气有毒,属于大气污染物,需要尾气处理,即应该在在丙装置后连接一个盛有氢氧化钠溶液的洗气瓶。
(3)次氯酸钙和碘化钾反应的方程式为ClO-+2I-+2H+=I2+Cl-+H2O,所以次氯酸钙和Na2S2O3的关系式为Ca(ClO)2~4Na2S2O3。所以25ml溶液中含有次氯酸钙的物质的量是0.1 mol/L×0.02L÷4=0.0005mol,质量是0.0005mol×143g/mol=0.0715g,所以质量分数是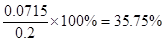 。
。
