(12分)某化学学习小组采用下图所提供的仪器装置(夹持仪器已略去)设计实验:验证浓硝酸的氧化性。实验表明浓硝酸能将NO氧化成NO2,由此得出的结论是浓硝酸具有氧化性。
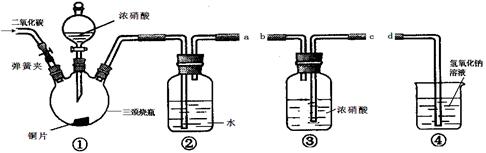
试回答有关问题:
(1)仪器接口的连接顺序为___________ ____________;
(2)按(1)中连接顺序安装好装置后下一步的操作是___ ____;
加入药品后,打开弹簧夹,通入CO2一段时间,通入CO2的目的是___________________________________________________;
关闭弹簧夹,将装置④中的导管末端伸入氢氧化钠溶液中是为了_________________ __________________;
(3)装置②发生反应的化学方程式是___________________________________;
(4)该小组得出的结论所依据的实验现象是_____________________________。
(1)a→c→b→d
(2)检验装置气密性;排尽装置中的空气;
吸收二氧化氮,防止其扩散到空气中污染空气
(3) 3NO2+H2O=2HNO3+NO (4)②中逸出的无色气体通过③时变成红棕色
(1)①是气体的发生装置,浓硝酸和铜反应生成NO2,NO2溶于水即生成NO,所以要检验浓硝酸的氧化性,需要把NO通入到浓硝酸中,氮的氧化物属于大气污染物,需要进行尾气处理,因此最后要通入到氢氧化钠溶液中,即顺序为a→c→b→d。
(2)装置连接好以后,必须最÷检验装置的气密性。因为空气中的氧气也能氧化NO,所以为了防止干扰,需要排尽装置中的空气。
(3)NO2溶于水的方程式为3NO2+H2O=2HNO3+NO。
(4)NO是无色,被氧化生成NO2后气体颜色变为红棕色,所以当②中逸出的无色气体通过③时变成红棕色,即说明结论是正确的。
