实验盒中有5种没有标签的溶液,老师让实验小组同学鉴别这些溶液。
【调查研究】
①实验盒中记录单上登记的5种溶液是:Na2CO3、CuSO4、Ca(OH)2、NaOH和稀盐酸,其中有颜色的是 溶液;
②查阅资料:无色有刺激性气味的氯化氢气体溶于水得到盐酸;
③研究方式:从4种无色溶液中任意取出3种为一组进行鉴别。
【提出假设】同学们从4种无色溶液中取出3种,贴上A、B、C标签,并且假设这一组溶液可能是Na2CO3、Ca(OH)2和NaOH。
【实验探究】同学们按以下步骤进行鉴别:
第一步 取3支试管,分别加入少量的A、B、C溶液,然后依次加入少量盐酸,实验现象记录如下:
| 溶液 | A | B | C |
| 加入盐酸后的现象 | 无明显变化 | 无明显变化 | 有气泡产生 |
第二步 依据如图装置进行实验,其中夹持固定装置已略去。从长颈漏斗加入盐酸,可以观察到C溶液中气泡产生,A溶液中有白色沉淀生成,B溶液无明显变化。
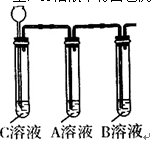
实验解释:
①A溶液中产生的白色沉淀是 (写出化学式),则A是 溶液。
②写出C溶液中发生反应的化学方程式 。
第三步 取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热。
实验结论:B是 溶液。
经过上述三步实验,同学们认为最后一种溶液是 溶液。
【实验反思】老师提出:鉴别出C溶液后,不需外加试剂,就可以简便地鉴别出A、B溶液。请完成下列实验报告
| 实验步骤 | 实验现象 | 结论 |
| 取A、B两溶液分别于两支试管中,各滴加C溶液 | _____________________ | 该溶液是A 溶液 |
| _____________________ | 该溶液是B溶液 | |
:21、(18分)【调查研究】CuSO4
【实验探究】Na2CO3
实验解释① CaCO3 Ca(OH)2 ?Na2CO3+2HCl=2NaCl+H2O+CO2↑
盐酸 NaOH
| 实验操作步骤 | 实验现象 | 实验结论 |
| 有白色沉淀产生 | ||
| 有气泡产生 |
分析:[调查研究]
常见溶液的颜色:可溶性铜盐溶液呈蓝色,可溶性亚铁盐溶液呈浅绿色,可溶性铁盐溶液呈黄色;
[实验探究]
滴加稀盐酸,发现溶液C与稀盐酸反应产生气体,在所给溶液中判断可与稀盐酸反应并生成气体的溶液;
实验解释
①根据通入二氧化碳气体,溶液出现沉淀判断所给溶液及沉淀;
②写出放出二氧化碳反应的化学方程式;
实验结论
溶液加热,闻到刺激性气味,据此分析所给溶液中受热会出现此现象的溶液;
[实验反思]
用碳酸钠溶液鉴别稀盐酸和氢氧化钙溶液,根据碳酸钠与两种溶液反应时不同的现象鉴别它们.解:[调查研究]
Na2CO3、CuSO4、Ca(OH)2、NaOH和稀盐酸五种溶液中,Na2CO3、Ca(OH)2、NaOH和稀盐酸为无色溶液,而CuSO4溶液为蓝色;
故选CuSO4
[实验探究]
Na2CO3、Ca(OH)2和NaOH三种溶液中,后两种溶液为碱溶液,可与稀盐酸发生中和反应生成盐和水,却无气体放出;而碳酸钠溶液可与稀盐酸反应放出气体二氧化碳;
故答:Na2CO3
实验解释
①在Ca(OH)2和NaOH溶液中,通入二氧化碳出现沉淀的溶液应为Ca(OH)2溶液,生成的沉淀为碳酸钙;
故选CaCO3,Ca(OH)2?
②C溶液为碳酸钠溶液,与滴入的稀盐酸发生复分解反应,生成氯化钠、水和气体二氧化碳;
故答:Na2CO3+2HCl=2NaCl+H2O+CO2↑
实验结论
在未确定的NaOH和稀盐酸两种溶液中,加热时能闻到刺激性气味的溶液为稀盐酸,稀盐酸受热挥发出HCl,HCl是一种有刺激性气味的气体;到此为止,实验盒中的五种溶液只剩下NaOH溶液还没进行鉴别,所以最后剩余的溶液就是NaOH溶液;
故答:盐酸,NaOH
[实验反思]
碳酸钠溶液与稀盐酸反应生成二氧化碳,可观察到有大量气泡;而碳酸钠与氢氧化钙溶液发生反应,生成不溶于水的碳酸钙,可观察到有白色沉淀产生;
故答:
| 实验步骤 | 实验现象 | 结论 |
| 有白色沉淀产生 | ||
| 有气泡产生 |
