问题
选择题
a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族,a的原子结构示意图为
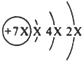
,b与c形成化合物的电子式为
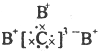
.下列比较中正确的是( )
A.原子半径:a>c>b
B.原子的氧化性:a>c>d
C.a的单质不能导电
D.最高价含氧酸的酸性c>d>a
答案
a的原子结构示意图为
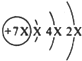
,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与c形成化合物的电子式为

,则b处于ⅠA族、c处于ⅤA族,c、d同主族,a、b、d同周期,故b为Na元素,则c为N元素,D为P元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,则原子半径Na>Si>N,故A错误;
B.氮气的性质稳定,氧化性比磷弱,故B错误;
C.硅是半导体,故C错误;
D.非金属性越强最高价含氧酸的酸性越强,非金属性N>P>Si,故最高价含氧酸的酸性c>d>a,故D正确;
故选D.
