现有A、B、C、D、E、F、G七种核电荷数小于18的元素,它们的原子序数一次递增.其中:A原子核内无中子,B原子最外层电子数是次外层的2倍,D原子最外层电子数是其电子层数的3倍,E原子核外第一层比第三层电子数多1,F的最外层电子数等于第一层电子数,G形成的-1价离子与Ar原子核外电子排布相同;
由此推知:
(1)A原子符号是______;
(2)B原子结构示意图是______
(3)G元素形成的单质与A、D、E三元素形成呈碱性的化合物反应的离子方程式:______
单质F分别在C单质、BD元素形成的化合物中燃烧的化学方程式:______;______.
A、B、C、D、E、F、G七种核电荷数小于18的元素,它们的原子序数依次递增.其中:A原子核内无中子,则A是H元素,B原子最外层电子数是次外层的2倍,则B是C元素,D原子最外层电子数是其电子层数的3倍,则D是O元素,C的原子序数大于B小于D,所以C是N元素,E原子核外第一层比第三层电子数多1,则E是Na元素,F的最外层电子数等于第一层电子数,且F的原子序数大于E,所以F是Mg元素,G形成的-1价离子与Ar原子核外电子排布相同,则G是Cl元素.
(1)因A为H元素,则A原子符号是11H,故答案为:11H;
(2)B为C元素,C原子结构示意图为
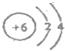
,故答案为:
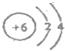
;
(3)G元素形成的单质是氯气,A、D、E三元素形成呈碱性的化合物是氢氧化钠,氯气和氢氧化钠溶液反应的离子方程式为:2OH-+Cl2═Cl-+ClO-+H2O,镁分别在氮气、二氧化碳中燃烧的化学方程式为:3Mg+N2
Mg3N2,2Mg+CO2 点燃 .
2MgO+C,故答案为:2OH-+Cl2═Cl-+ClO-+H2O;3Mg+N2 点燃 .
Mg3N2;2Mg+CO2 点燃 .
2MgO+C. 点燃 .
