实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)、 配制250mL0.1mol/L的盐酸溶液
| 应称量盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需的其它仪器 |
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)、操作A中,将洗涤液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢复到室温,这是因为_____________________;
(4)、若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响” )
若没有进行A操作 ;若加蒸馏水时不慎超过了刻度 ;
若定容时俯视刻度线 _______________。
(5)、若实验过程中出现如下情况如何处理?
加蒸馏水时不慎超过了刻度 ;
向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面 。
(1)2.1,250,量筒、烧杯、玻璃棒、胶头滴管。
(2)B、C、A、F、E、D
(3)保证溶质全部转入容量瓶。容量瓶盛放热溶液时,体积不准,也易导至容量瓶炸裂。
(4)浓度偏低;偏低;偏高。
(5)宣告实验失败,洗净容量瓶后重新配制;宣告实验失败,洗净容量瓶后重新配制。
题目分析:(1)浓盐酸的浓度为c= ,要配置250mL0.1mol/L的盐酸溶液需要用浓盐酸的体积为V=
,要配置250mL0.1mol/L的盐酸溶液需要用浓盐酸的体积为V=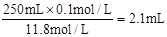 。应该选用250mL容量瓶,配置溶液时除了需要250mL容量瓶外,还需要量筒、烧杯、玻璃棒、胶头滴管。
。应该选用250mL容量瓶,配置溶液时除了需要250mL容量瓶外,还需要量筒、烧杯、玻璃棒、胶头滴管。
(2)配置一定物质的量浓度溶液的过程为:计算、量取、稀释、转移、洗涤、定容、摇匀和装瓶贴签,所以应该正确的操作顺序为B、C、A、F、E、D。
(3)将洗涤液全部转入容量瓶中的目的是保证溶质全部转移到容量瓶。注入容量瓶前需要恢复到室温是因为容量瓶盛放热溶液时,当溶液冷却到室温的时候,体积会缩小,不准确,也易导至容量瓶炸裂。
(4)根据c= ,如果没有洗涤,则溶质的物质的量比正常值小,所以浓度偏低;若加蒸馏水不慎超过刻度,溶液的体积比正常值大,所以浓度偏低;若定容时俯视刻度线,则溶液的体积比正常值小,则浓度偏高。
,如果没有洗涤,则溶质的物质的量比正常值小,所以浓度偏低;若加蒸馏水不慎超过刻度,溶液的体积比正常值大,所以浓度偏低;若定容时俯视刻度线,则溶液的体积比正常值小,则浓度偏高。
(5)如果加水不慎超过了刻度线,则需要将溶液倒掉,洗净容量瓶重新配置,如果转移时不慎有液体滴在外面则需要将溶液倒掉,洗净容量瓶重新配置。
点评:本题比较基础,主要考查学生的基本实验操作。
