氮元素十分重要,其单质及其化合物在科研、生产领域有着十分广泛的用途。
(1)氮元素核外电子排布式为: ,原子核外共有 种不同能级的电子,氮原子核外电子云有 种不同的伸展方向,有 种不同运动状态的电子。
(2)最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:
2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) - Q ,如果反应的平衡常数K值变大,该反应 (选填编号)。
4NH3 (g)+3O2 (g) - Q ,如果反应的平衡常数K值变大,该反应 (选填编号)。
A.一定向正反应方向移动
B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动
D.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中进行,当反应达到平衡后,下列判断错误的是
A.容器中气体的平均分子量不随时间而变化 B.通入大量稀有气体能提高反应的速率
C.容器中气体的密度不随时间而变化 D.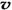 (N2)/
(N2)/ 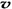 (O2)=2:3
(O2)=2:3
(4)高氯酸铵作为火箭燃料的重要氧载体。高氯酸铵在高压、450℃的条件下迅速分解,反应的化学方程式4NH4ClO4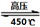 6H2O↑+ 2N2↑+ 4HCl↑+ 5O2↑,其中氧化产物与还原产物的物质的量之比是 ,每分解1mol高氯酸铵,转移的电子数目是 。
6H2O↑+ 2N2↑+ 4HCl↑+ 5O2↑,其中氧化产物与还原产物的物质的量之比是 ,每分解1mol高氯酸铵,转移的电子数目是 。
(1) 1s22s22P3 , 3, 4, 7
(2)AB
(3)B
(4) 7∶4 8NA 或 4.816×1024 个
题目分析:(1)氮元素是7号元素核外电子有7个,排布式为:1s22s22P3 ,由于有三种能级,故原子核外共有3种不同能级的电子,氮原子核外电子云有的伸展方向s是球形的只有一种,P轨道有3种,共有4伸展方向。由于同一轨道上的两个电子自旋方向不同,故共有7种不同运动状态的电子。
(2)2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) - Q ,正反应是吸热反应,如果反应的平衡常数K值变大,则生成物浓度增大,反应物浓度减小,则有 A.一定向正反应方向移动,正确。B.在平衡移动时正反应速率先增大后减小,说明平衡右移,正确。
4NH3 (g)+3O2 (g) - Q ,正反应是吸热反应,如果反应的平衡常数K值变大,则生成物浓度增大,反应物浓度减小,则有 A.一定向正反应方向移动,正确。B.在平衡移动时正反应速率先增大后减小,说明平衡右移,正确。
(3)相当于在恒容容器中,A.容器中气体的平均分子量不随时间而变化,说明达到了平衡,正确。 B.通入大量稀有气体各物质的量浓度没有改变,反应的速率不改变,错误。C.由于反应前后气体的质量不等,所以容器中气体的密度不随时间而变化可以做为平衡判断的依据,正确。D.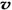 (N2)/
(N2)/ 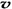 (O2)=2:3,速率之比等于化学计量数之比,正确。
(O2)=2:3,速率之比等于化学计量数之比,正确。
(4)该反应4NH4ClO4 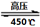 6H2O↑+ 2N2↑+ 4HCl↑+ 5O2↑中,氧化产物是氮气和氧气,还原产物是氯化氢,物质的量之比是 7∶4 ,每分解1mol高氯酸铵,转移的电子数目是 8NA 或 4.816×1024 个。
6H2O↑+ 2N2↑+ 4HCl↑+ 5O2↑中,氧化产物是氮气和氧气,还原产物是氯化氢,物质的量之比是 7∶4 ,每分解1mol高氯酸铵,转移的电子数目是 8NA 或 4.816×1024 个。
