单质碘与红磷在常温下混合不反应,但滴入几滴水后能剧烈反应,生成HI和H3PO3。但实验室制取氢碘酸的方法是把H2S通入I2水中,过滤生成的硫,可得质量分数为50%的氢碘酸
(1)写出实验室制取氢碘酸的化学方程式______________________;
(2)氢碘酸在空气中放置易易氧化变质,写出可能发生反应的化学方程式___________________________;
(3)为防止氢碘酸在空气中氧化变质,可在氢碘酸中加入少量___________,写出有关反应的化学方程式__________________________。
(4)在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表:
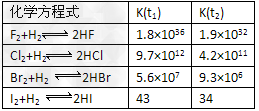
①已知t2>t1,HX的生成反应是__________ 反应(填“吸热”或“放热”)。
②共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是_______________。
③仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_________________(选填字母)。
a.在相同条件下,平衡时X2的转化率逐渐降低
b.X2与H2反应的剧烈程度逐渐减弱
c.HX的还原性逐渐减弱
d.HX的稳定性逐渐减弱
(1)I2+H2S==2HI+S↓
(2)4HI+O2==I2+2H2O
(3)红磷;3I2+2P+3H2O==6HI+2H3PO3
(4)①放热;②HF、HCl、HBr、HI;③ad
