研究碳及其化合物的综合利用对促进低碳社会的构建具有重要的意义。请运用相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:______C+________K2Cr2O7+________——________CO2↑+________K2SO4+________Cr2(SO4)3+________H2O。
①完成并配平上述化学方程式。
②在上述化学方程式上标出该反应电子转移的方向与数目。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是_________________________________________________________。
②由MgO可制成“镁-次氯酸盐”燃料电池,其装置示意图如图(a)所示,该电池反应的离子方程式为________________________________________。
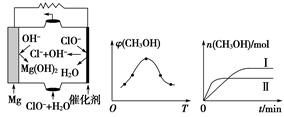
(a) (b) (c)
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH。
CH3OH(g)+H2O(g) ΔH。
①该反应的平衡常数表达式为K=________。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图(b)所示,则上述CO2转化为甲醇反应的ΔH________(填“>”“<”或“=”)0。
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图(c)所示,曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ________KⅡ(填“>”“<”或“=”)。
(1)①3 2 8 H2SO4 3 2 2 8
② +8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
(2)①2MgSO4+CO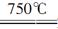 2MgO+SO2+CO2+SO3
2MgO+SO2+CO2+SO3
②Mg+ClO-+H2O=Cl-+Mg(OH)2
(3)①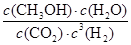 ②< ③>
②< ③>
(1)①反应中C→CO2,化合价升高4,K2Cr2O7→Cr2(SO4)3,化合价降低6,根据得失电子守恒、质量守恒定律即可配平反应的化学方程式。
②得失电子的最小公倍数为12,用单线桥或双线桥表示均可,单线桥表示如下:
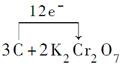 +8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
(2)①CO作还原剂,反应中CO→CO2,化合价升高2,MgSO4→SO2,化合价降低2,据此即可配平化学方程式。
②从图(a)可知,放电时Mg→Mg(OH)2,化合价升高2;ClO-+H2O→Cl-+OH-,化合价降低2,由此可配平反应的化学方程式。
(3)①平衡常数为生成物浓度幂之积与反应物浓度幂之积的比值。
②从图(b)的最高点(平衡点)之后看,随着反应的进行,升高温度,平衡逆向移动,故正反应为放热反应,ΔH<0。
③从图(c)看,反应Ⅰ中生成甲醇的物质的量大于反应Ⅱ中生成甲醇的物质的量,说明Ⅰ条件下有利于平衡正向移动,平衡常数大。
