.

Changed Lives
In 1921, Lewis Lawes became the warden(监狱长) at Sing Sing Prison. No prison was kept 1 than Sing Sing during that time. But 20 years later, it had become a 2 place. When he was asked about the change, here's what he said, "I 3 it all to my wonderful wife, Catherine, who is 4 outside the prison walls."
Catherine Lawes was a young mother. Everybody 5 her from the beginning that she should never 6 foot inside the prison walls, but that didn’t 7 her! When the first prison basketball game was held, she went into the gym with her three beautiful kids and she sat in the stands with the prisoners.
She 8 getting to know them and their records. She 9 one convicted murderer was blind so she paid him a visit. 10 his hand in here she said, "Do you read Braille(布莱叶盲文)?" "What’s Braille?" he asked. Then she taught him how to read. Years later he would 11 in love for her.
Then, she was killed in a car accident. The next morning Lewis Lawes didn’t come to work, so the acting(代理) warden took his place. It seemed almost 12 that the prison knew something was 13 .
The following day , her body was resting in a casket(灵柩) in her home. 14 the acting warden took his early morning walk, he was 15 to see a large crowd of the toughest, hardest-looking prisoners 16 like a crowd of animals at the main gate. He came closer and 17 tears of grief(悲恸) and sadness. He turned and faced the men, "All right, men you can go. Just be sure and 18 tonight!" Then he opened the gate and a parade of prisoners 19 , without a guard, the three-quarters of a mile to stand in line to 20 their final respects to Catherine Lawes.
And every one of them came back . Every one!
1. A. better B. harder C. older D. tougher
2. A. beautiful B. wonderful C. humanitarian D. attractive
3. A. belong B. give C. contribute D. owe
4. A. working B. supporting C. buried D. located
5. A. warned B. told C. reminded D. informed
6. A. put B. lay C. set D. get
7. A. persuade B. stop C. keep D. submit
8. A. insisted on B. hold out C. carry out D. keep up
9. A. searched B. thought C. discovered D. caught
10. A. Shaking B. Putting C. Feeling D. Holding
11. A. laugh B. weep C. appreciate D. touch
12. A. long B. apparently C. immediately D. later
13. A. changeable B. disappointing C. mad D. wrong
14. A. As B. Once C. While D. Since
15. A. glad B. angry C. shocked D. frightened
16. A. rushed B. shouted C. waited D. gathered
17. A. noticed B. found C. expected D. understood
18. A. check on B. check in C. check out D. check through
19. A. escaped B. walked C. fled D. hurried
20. A. attribute B. take C. pay D. display

 H2↑ + Cl2↑ + 2OH-(2分)
H2↑ + Cl2↑ + 2OH-(2分)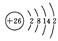
 H2↑ + Cl2↑ + 2OH-;
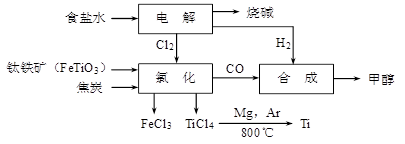
H2↑ + Cl2↑ + 2OH-; H2↑ + Cl2↑ + 2OH-;再根据图示可知氯化时的反应物为FeTiO3、C、Cl2,生成物为FeCl3、TiCl4、CO,再根据得失电子和原子守恒即可得出该反应的方程式为2FeTiO3+6C+
H2↑ + Cl2↑ + 2OH-;再根据图示可知氯化时的反应物为FeTiO3、C、Cl2,生成物为FeCl3、TiCl4、CO,再根据得失电子和原子守恒即可得出该反应的方程式为2FeTiO3+6C+ 2FeCl3+2TiCl4+6CO,得出关系式2FeTiO3 ~ 7Cl2 ~ 14NaCl,所以为了减少产业链生产时产生的工业三废对环境的威胁,当NaCl与FeTiO3的物质的量之比为7:1时,理论上Cl2的利用率最大。
2FeCl3+2TiCl4+6CO,得出关系式2FeTiO3 ~ 7Cl2 ~ 14NaCl,所以为了减少产业链生产时产生的工业三废对环境的威胁,当NaCl与FeTiO3的物质的量之比为7:1时,理论上Cl2的利用率最大。
