问题
填空题
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50 ℃时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是2Cu+ Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答:
Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 。
(2)写出CuH在氯气中燃烧的化学反应方程式
(3)CuH溶解在稀盐酸中生成的气体是 ,如果反应中生成了标准状况下22.4 L的气体,被还原的离子得电子的物质的量是 。
答案
(1)还原剂
(2)2CuH+3Cl2 2CuCl2+2HCl
2CuCl2+2HCl
(3)H2 1.5 mol
(1)Cu2+ Cu+,铜元素化合价降低,被还原,所以加入的应该是还原剂。
Cu+,铜元素化合价降低,被还原,所以加入的应该是还原剂。
(2)CuH在氯气中能燃烧,铜元素和氢元素都被氯气氧化,故可推知产物为氯化铜和氯化氢,根据得失电子守恒和原子守恒就可以配平反应方程式。
(3)CuH溶解在稀盐酸中,氢元素发生归中反应,生成的气体为氢气,同时根据信息Cu+在酸性条件下发生的反应是2Cu+ Cu2++Cu,综上所述总化学方程式是:2CuH+2HCl
Cu2++Cu,综上所述总化学方程式是:2CuH+2HCl CuCl2+Cu+2H2↑,
CuCl2+Cu+2H2↑,
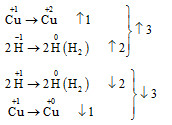
则生成2 mol H2时,转移电子3 mol,生成1 mol H2时,转移电子为1.5 mol。
