工业上用硫碘开路循环联产氢气和硫酸的工艺流程如图所示:
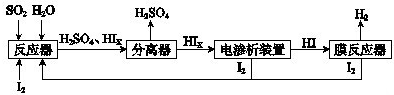
请回答下列问题:
(1)在反应器中发生反应的化学方程式是______.
(2)在膜反应器中发生反应:2HI(g)⇌H2(g)+I2(g)△H>0.若在一定条件密闭容器中加入1mol HI(g),n(H2)随时间(t)的变化关系如图1所示:
①该温度下,反应平衡常数K=______,若升高温度,K值将______(填“增大”、“减小”或“不变”).
②用化学平衡原理解释使用膜反应器及时分离出H2的目的是______.
(3)电渗析装置如图2所示:
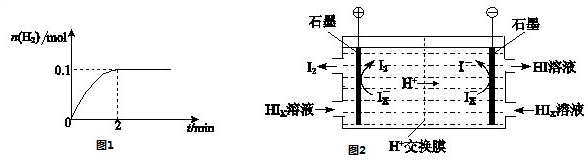
①结合电极反应式解释阴极区HIx转化为HI的原理是______.
②该装置中发生的总反应的化学方程式是______.
(4)上述工艺流程中循环利用的物质是______.
(1)由工艺流程图可知,SO2、I2、H2O反应生成H2SO4、HIX,反应方程式为:SO2+x I2+2H2O═H2SO4+2HIX,故答案为:SO2+x I2+2H2O═H2SO4+2HIX;
(2)①由图1可知,平衡时氢气的物质的量为0.1mol,则:
2HI(g)⇌H2(g)+I2(g)
开始(mol):1 0 0
变化(mol):0.2 0.1 0.1
平衡(mol):0.8 0.1 0.1
由于反应前后气体的物质的量不变,故可以利用物质的量代替浓度计算平衡常数,故k=
=0.1×0.1 0.82
,1 64
该反应正反应是吸热反应,升高温度,平衡向正反应移动,平衡常数增大,
故答案为:
;增大;1 64
②使用膜反应器及时分离出H2,使平衡正向移动,提高HI的分解率,故答案为:使平衡正向移动,提高HI的分解率;
(3)①由图2可知,在阴极区Ix-转化为I-,发生反应:Ix-+(x-1)e-═xI-,且阳极区的H+通过交换膜进入阴极区,得以生成HI溶液,
故答案为:在阴极区发生反应:Ix-+(x-1)e-═xI-,且阳极区的H+通过交换膜进入阴极区,得以生成HI溶液;
②由图2可知,在阴极区Ix-转化为I-,在阳极区Ix-转化为I2,阳极区的H+通过交换膜进入阴极区,得以生成HI溶液,即电解HIx生成I2、HI,反应方程式为:2HIx═(x-1)I2+2HI,
故答案为:2HIx═(x-1)I2+2HI;
(4)由工艺流程可知,电渗析装置与膜反应器中都产生I2,可以在反应器中循环利用,故答案为:I2.
