问题
选择题
工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对人类及生态系统产生很大的危害,必须进行处理。下面是一种处理方法的工业流程:
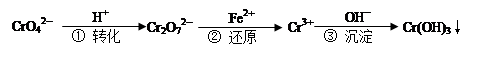
下列说法正确的是:
A.改变反应①的平衡体系中c(H+)浓度,溶液颜色无明显变化
B.若2v (Cr2O72—) ="v" (CrO42—),说明反应①达平衡状态
C.反应②中还原1mol Cr2O72—,需要6 mol的Fe2+
D.FeSO4溶液呈酸性的原因是Fe2++ 2H2O  Fe(OH) 2↓+ 2H+
Fe(OH) 2↓+ 2H+
答案
答案:C
题目分析:依据化学平衡影响因素分析,氢离子浓度增大平衡正向进行,溶液颜色发生变化,变橙色,氢离子浓度减 * * 衡逆向进行,溶液呈黄色,故A错误;化学反应速率之比等于化学方程式中计量数之比,是正反应速率之比,不能证明反应达到平衡,故B错误;依据氧化还原反应电子守恒计算,Cr2O72-,~2Cr3+~6e-;Fe2+~Fe3+~e-,还原1mol Cr2O72-,需要6mol的Fe2+,故C正确;亚铁离子水解程度微弱不能生成氢氧化亚铁沉淀,反应过程是可逆反应,反应的离子方程式为:Fe2++2H2O?Fe(OH)2+2H+,故D错误,故选C。
