问题
选择题
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O;NO+NO2+2NaOH=2NaNO2+H2O。
则生成的盐溶液中NaNO2的物质的量为
A.0.4 mol
B.0.6 mol
C.0.8 mol
D.0.2 mol
答案
答案:C
反应中Cu-2e-—→Cu2+,NO—→NO、NO2、N2O4—→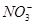 +
+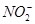 ,从电子守恒可知,铜失去的电子数与
,从电子守恒可知,铜失去的电子数与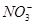 变成
变成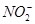 过程中得到的电子数相等,
过程中得到的电子数相等,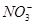 +2e-+2H+=
+2e-+2H+=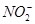 +H2O,故生成NaNO2的物质的量与铜的物质的量相等:
+H2O,故生成NaNO2的物质的量与铜的物质的量相等: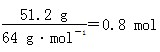 ,C项正确。
,C项正确。
