问题
填空题
(I)在铝热反应 Fe2O3+2Al
2Fe+Al2O3 中,作为氧化剂的物质是______(填化学式),作为还原剂的物质是______(填化学式); 高温 .
(II)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快.由此判断,影响化学反应速率的因素有______和______;
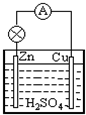
(III)原电池是一种将______能转化为______能的装置.在Cu-Zn原电池中,Zn极发生______反应,电极反应式为______.
答案
(I)Fe2O3+2Al
2Fe+Al2O3,该反应中元素的化合价变化为:Fe2O3→Fe,铁元素由+3价→0价,得电子发生还原反应,所以Fe2O3是氧化剂;Al→Al2O3,铝元素由0价→+3价,失电子发生氧化反应,所以Al是还原剂. 高温 .
故答案为:Fe2O3;Al.
(II)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快.根据此现象判断,反应速率与反应物的浓度、温度有关.
故答案为:温度;浓度.
(III)原电池的定义:把化学能转变为电能的装置;在Cu-Zn原电池中,Zn失电子变成离子进入溶液,所以锌发生氧化反应,电极反应式为Zn-2e-=Zn2+;
故答案为:化学;电;氧化;Zn-2e-=Zn2+.
