水在很多的反应中,起到极其重要的作用.根据下面水参与的反应,回答问题:
①2F2+2H2O═4HF+O2 ②2Na2O2+2H2O═4NaOH+O2↑
③2Na+2H2O═2NaOH+H2↑ ④2H2O
2H2↑+O2↑ 电解 .
(1)水只作氧化剂的是______;(填写序号,下同)水只作还原剂的是______;水既作氧化剂,又做还原剂的是______;水既不是氧化剂,又不是还原剂的氧化还原反应是______.
(2)请标出下列反应的电子转移的方向和数目.
3Cl2+6NaOH=5NaCl+NaClO3+3H2O
(3)上述反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O若转移5mol电子,则所得氧化产物的物质的量为______mol.
(1)①该反应中,水中O元素失电子化合价升高,所以水中还原剂;
②该反应中水中的H和O元素的化合价都不变,所以水既不是氧化剂又不是还原剂;
③该反应中钠失电子化合价升高,水中氢元素得电子化合价降低,所以水作氧化剂;
④该反应中,水中的H元素得电子化合价降低,水中的O元素失电子化合价升高,所以水既是氧化剂又是还原剂;
故答案为:③;①;④;②;
(2)反应3Cl2+6NaOH(热,浓)═5NaCl+NaClO3+H2O中,化合价升高的元素是Cl,化合价降低的元素也是氯元素,化合价升高数目=化合价降低数目=转移电子数目=5,电子转移的方向和数目如下所示:
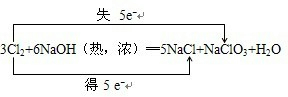
,
故答案为:

;
(3)该反应中的氧化产物是氯酸钠,氯酸钠和转移电子之间的关系式是1:5,所以若转移5mol电子,则所得氧化产物的物质的量为1mol,故答案为:1.
