二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.
工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
①CO( g)+2H2(g)⇌CH3OH( g)△H1=-91KJ•mol-1
②2CH30H(g)⇌CH30CH3(g)+H20(g)△H2=-24KJ•mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41KJ•mol-1
回答下列问题:
(1)新工艺的总反应为:3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H该反应△H=______,平衡常数表达式K=______
(2)增大压强,CH30CH3的产率______(填“增大”、“减小”或“不变”).
(3)原工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.新工艺中反应③的发生提高了CH30CH3的产率,原因是______.
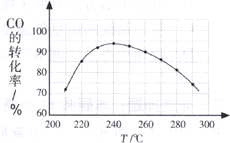
(4)为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是______,其原因是______.
(1)已知①CO( g)+2H2(g)⇌CH3OH( g)△H1=-91KJ•mol-1,
②2CH30H(g)⇌CH30CH3(g)+H20(g)△H2=-24KJ•mol-1,
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41KJ•mol-1,
根据盖斯定律,①×2+②+③得3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g)△H=-247KJ•mol-1,
平衡常数指产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,所以k=
,c(CH3OCH3)•c(CO2) c3(CO)•c3(H2)
故答案为:-247KJ•mol-1;
;c(CH3OCH3)•c(CO2) c3(CO)•c3(H2)
(2)反应前后气体的气体减小,增大压强平衡向体积减小的方向移动,即向正反应方向移动,CH30CH3的产率增大,故答案为:增大;
(3)反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率,
故答案为:反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
(4)由图表可知,温度低于240℃时,CO的转化率随着温度的升高而增大;温度高于240℃时,CO的转化率随着温度的升高而减小,
在较低温时,各反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应速率增大,CO的转化率也增大;在较高温时,各反应体系均已达到平衡,CO的转化率主要受反应限度影响,随着温度的升高平衡向逆反应方向移动,CO的转化率减小,
故答案为:温度低于240℃时,CO的转化率随着温度的升高而增大;温度高于240℃时,CO的转化率随着温度的升高而减小;
在较低温时,各反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应速率增大,CO的转化率也增大;在较高温时,各反应体系均已达到平衡,CO的转化率主要受反应限度影响,随着温度的升高平衡向逆反应方向移动,CO的转化率减小.