用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
⑴准确称取烧碱样品4.100g,将样品配成250mL的待测液,需要的仪器有小烧杯、量筒、玻璃棒、 __________、__________、___________ 。(填仪器)
⑵取10.00mL待测液,用__________量取注入锥形瓶中。(填仪器)
⑶用0.2010mol/L标准盐酸溶液滴定待测烧碱溶液,滴定时左手__________,右手__________,两眼注视__________,直到滴定终点。
(4)根据下列测定数据,分析得到合理数据,计算待测烧碱溶液的浓度:__________。
| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.52 |
| 第二次 | 10.00 | 4.00 | 23.08 |
| 第三次 | 10.00 | 4.20 | 26.70 |
(14分)(1)250mL容量瓶,胶头滴管、天平等(3分)
(2)可用碱式滴定管来量取,也可使用移液管来量取(2分)
(3)滴定过程中,滴定时左手控制活塞,右手不停地振荡锥形瓶,两眼注视锥形瓶中溶液颜色的变化,直到滴定终点。(3分)
(4)V(NaOH)=10.00mL V(HCl)=[(20.52mL-0.50mL)+(23.08mL-4.00)]/2=20.00mL
根据:c(NaOH)V(NaOH)=c(HCl)V(HCl) 则:c(NaOH)=0.4020mol/L(3分)
(5)样品中m(NaOH)=0.4020mol/L×0.250L×40g/mol=4.02g
则烧碱的纯度为:4.02g/4.1g×100%=98.05% (3分)
题目分析:(1)配成250mL的待测液,需要的仪器除小烧杯、量筒、玻璃棒外,还有250mL容量瓶,胶头滴管、天平等。
(2)氢氧化钠溶液显碱性,所以取10.00mL待测液,应该用碱式滴定管来量取,也可使用移液管来量取注入锥形瓶中。
(3)用0.2010mol/L标准盐酸溶液滴定待测烧碱溶液,滴定时左手控制活塞,右手不停地振荡锥形瓶,两眼注视锥形瓶中溶液颜色的变化,直到滴定终点。
(4)根据表中数据可知,三次实验中消耗盐酸的体积是20.02ml、19.08ml、22.5ml,显然第三次实验中误差太大,舍去。则消耗盐酸体积的平均值是(20.02ml+19.08)÷2=20.00ml,则待测烧碱溶液的浓度是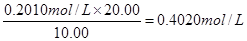
(5)样品中m(NaOH)=0.4020mol/L×0.250L×40g/mol=4.02g
则烧碱的纯度为:4.02g/4.1g×100%=98.05%
点评:该题是中等难度的试题,试题基础性强,难易适中,贴近高考。该题在注重对学生基础性知识巩固与训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和灵活应变能力,提升学生的学科素养。
