I甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:
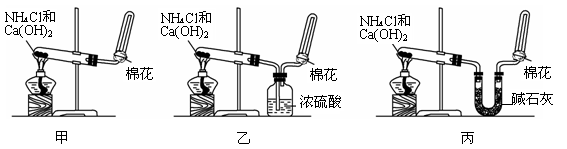
(1)三位同学制取氨气的化学方程式为:_____________________________________________。
(2)三位同学用上述装置制取氨气时,其中乙同学没有收集到氨(如果他们的实验操作都正确),你认为收集不到氨气的主要原因是_____________________________________(用化学方程式表示)。
(3)检验氨气是否收集满的方法是(简述操作方法、现象和结论)_______________________
II某校化学小组学生设计如图装置(图中铁夹等夹持装置已略去)进行氨气催化氧化的实验。
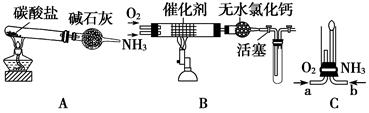
(4)用装置A制取纯净、干燥的氨气,大试管内是碳酸盐;碱石灰的作用是__________________________________。
(5)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:氨催化氧化的化学方程式是_______________;试管内气体变为红棕色,该反应的化学方程式是_________________。
1)2NH4Cl + Ca(OH)2 ==CaCl2 + 2NH3↑+ 2H2O
(2) 2NH3 + H2SO4 =(NH4)2SO4
(3)将湿的红色石蕊试纸放在管口;变蓝则已满
(4)吸收CO2和水蒸气
(5)4NH3 + 5O2 ="==4NO" + 6H2O 2NO + O2 =2NO2
题目分析:(1)三位同学都是利用氯化铵与氢氧化钙反应制备氨气,其化学方程式为
2NH4Cl + Ca(OH)2 ==CaCl2 + 2NH3↑+ 2H2O;(2)氨气能够与浓硫酸反应,所以乙同学收不到氨气,即发生了如下反应:2NH3 + H2SO4 =(NH4)2SO4 ;(3)检验氨气是否收集满的方法是:将湿的红色石蕊试纸放在管口;变蓝则已满;(4)由碳酸盐与氯化铵反应生成了二氧化碳和水,所以碱石灰的作用是吸收CO2和水蒸气;(5)氨催化氧化的化学方程式是:4NH3 + 5O2 ="==4NO" + 6H2O,NO可以被氧气氧化为红棕色的二氧化氮,其化学方程式为2NO + O2 =2NO2。
点评:本题考查了实验室制备氨气的基础知识,是高考考查的重点,本题不难。

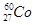 的衰变方程式为
的衰变方程式为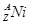 +
+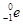 +Ve,其中Ve是反中微子,它的电荷为零,静止质量可以为零。
+Ve,其中Ve是反中微子,它的电荷为零,静止质量可以为零。