现有A、B、C、D、E五种元素,它们的质子数依次增多.
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1.试回答:
(1)B是______、E是______.(写元素名称):
(2)B的离子结构示意图______,D的单质分子的电子式______,C元素最高价氧化物的水化物的电子式______.
(3)用电子式表示H2A形成过程:______
(4)写出CD的溶液中通入氯气的离子方程式:______
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性:______.
A、B、C、D、E五种元素,它们的质子数依次增多.
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体,则A为氧元素;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱,则B为铝元素;
③B为铝元素,C+离子比B3+离子多8个电子,则C为钾元素;
④C与D元素可以形成化合物CD,⑤CD的溶液中通入氯气后加淀粉溶液显蓝色,则D为碘元素;
⑥C为钾元素,在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1,则E为+1价金属,与钾元素同主族,则E为Cs元素.
(1)由上述分析可知,B是铝元素,E是铯元素,故答案为:铝;铯;
(2)B是铝元素,铝离子有2个电子层,核内质子数为13,最外层有8个电子,铝离子结构示意图
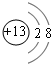
;
D为碘元素,D的单质分子的电子式为
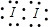
;C为钾元素,C元素最高价氧化物的水化物为KOH,电子式为
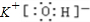
,
故答案为:

;
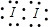
;
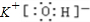
;
(3)A为氧元素,用电子式表示H2O形成过程为
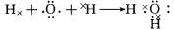
,
故答案为:
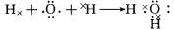
;
(4)氯气具有强氧化性,KI溶液中通入氯气,氯气将碘离子氧化为碘单质,反应的离子方程式2I-+Cl2═I2+2Cl-,故答案为:2I-+Cl2═I2+2Cl-;
(5)B是铝元素,C为钾元素,D是铯元素,金属性Al<K<Cs,所以B、C、E三种元素形成的简单离子氧化性Al3+>K+>Cs+,
故答案为:Al3+>K+>Cs+.
