问题
选择题
物质R在0.96 g氧气中恰好完全燃烧,反应方程式为:R+3O2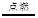 :XO2+2SO2,测得XO2和SO2的质量分别为0.44 g和1.28 g。下列判断正确的是
:XO2+2SO2,测得XO2和SO2的质量分别为0.44 g和1.28 g。下列判断正确的是
A.参加反应的R的质量为0.86 g
B.R的相对分子质量为76
C.R中含有X元素、S元素和O元素
D.XO2和SO2都是形成酸雨的主要物质
答案
答案:B
题目分析:依据质量守恒定律化学反应前后物质的总质量不变可知参加反应的R的质量为:1.28g+0.44g-0.96g=0.76g,A错误;设R的相对分子质量为X,则根据方程式计算
R+3O2=XO2+2SO2
X 96
0.76 0.96
x=96*0.76/96=76,B正确;
在化学反应中物质的质量比即为相对分子质量之比,那么XO2的相对分子质量为44,可能是二氧化碳;根据质量守恒定律化学反应前后元素的种类和质量不变,生成物中氧元素的质量=0.32g+0.64g=0.96g,等于反应物中氧气的质量,那么R中含有X元素、S元素,不含氧元素,C错误;二氧化碳主要是造成温室效应,D错误。故选B。
