医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:
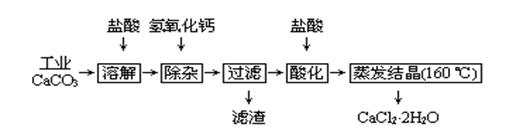
已知:查阅资料得知氢氧化物沉淀时的pH为:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀时的pH | 2.3 | 4.0 | 开始溶解:7.8 |
| 完全沉淀时的pH | 3.7 | 5.2 | 完全溶解:10.8 |
(1)CaCO3与盐酸反应的离子方程式 。
(2)除杂操作是加入氢氧化钙,调节溶液的pH为 ,目的是除去溶液中少量的Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是
。
(3)过滤时需用的玻璃仪器有 。滤渣主要成分的化学式 。
(4)酸化时加盐酸的目的为:① ,②防止Ca2+ 在蒸发时发生水解。
(5)为什么蒸发结晶要保持在160℃: 。
(6)测定晶体样品的纯度:若用一定浓度的AgNO3溶液滴定一定质量的晶体样品,所测样品中CaCl2 ·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为 。
(16分,每空2分)
(1)CaCO3+2H+=Ca2++CO2↑+H2O
(2)5.2~7.8(或之间的任意值、5.2≤pH<7.8) 静置,取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全;反之,则Fe(OH)3沉淀不完全
(3) 烧杯、玻璃棒、普通漏斗 Fe(OH)3、Al(OH)3
(4)除去过量的氢氧化钙(或防止氢氧化钙吸收空气中的二氧化碳,防止钙离子水解等,合理则给分)
(5)温度太高CaCl2 ·2H2O会失水
(6) Na+没除去析出NaCl,导致测定结果偏高(或少量CaCl2 ·2H2O失水)
题目分析:(1)盐酸是强酸,酸性比碳酸强,则难溶于水的碳酸钙易溶于盐酸,生成可溶性的氯化钙、二氧化碳气体和水,将易溶且易电离的化合物改写成离子形式,其余物质都保留化学式,删去实际上未反应的离子,则该反应为CaCO3+2H+=Ca2++CO2↑+H2O;(2)根据表中氢氧化物完全沉淀时的pH可知,除去溶液中少量铁离子和铝离子应使溶液pH介于5.2~7.8之间或者5.2≤pH<7.8,低于3.7时铁离子不能完全变为氢氧化铁沉淀,低于5.2时铝离子不能完全变为氢氧化铝沉淀,高于7.8时,氢氧化铝开始变为偏铝酸根离子,溶液又引入新的杂质;检验氢氧化铁是否沉淀的方法就是检验溶液中是否存在铁离子,由于铁离子遇KSCN溶液变红的特征反应,通常设计的实验方案为:静置,取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全,反之,则Fe(OH)3沉淀不完全;(3)过滤属于化学实验基本操作,也是混合物分离与提纯的常用方法,主要使用烧杯、玻璃棒、普通漏斗等仪器;当溶液pH介于5.2~7.8之间时,铁离子、铝离子完全变为氢氧化铁沉淀、氢氧化铝沉淀,则过滤所得滤渣的成分为Fe(OH)3、Al(OH)3;(4)氢氧化钙是除杂试剂,除杂试剂一定过量,氢氧化钙是强碱,由于目标产物是氯化钙,则酸化时加入盐酸的目的是除去过量的氢氧化钙,将其转化为氯化钙,防止氢氧化钙吸收空气中的二氧化碳,且过量的盐酸受热易挥发逸出(逸出的氯化氢气体可循环利用),不能加硝酸或硫酸酸化,因为它们除去旧杂质时会引入硝酸根离子或硫酸根离子等新杂质;(5)结晶水化合物受热可能失去结晶水,蒸发结晶要控制温度在160℃的原因是,温度太高,二水合氯化钙会失去结晶水;(6)滴定原理为:Ag++Cl-=AgCl↓,若氯离子的物质的量偏大,则测定结果偏高;酸化后所得溶液主要含有氯化钙、氯化钠、氯化氢,蒸发结晶时逸出氯化氢,但是没有除去钠离子,则所得晶体是二水合氯化钙和氯化钠的混合物,氯元素的质量分数:CaCl2>NaCl> CaCl2•H2O >CaCl2•2H2O,因此晶体样品中含有NaCl或二水合氯化钙失去全部或部分结晶水得到的CaCl2或CaCl2•H2O,都能导致所含氯元素的质量分数偏高,则所测样品二水合氯化钙的质量分数偏高。
