二氧化氯(ClO2)是一种广谱、高效的杀菌消毒剂,有与氯气相似的强烈刺激性气味,易溶于水,沸点11℃,遇热不稳定易分解发生爆炸。一种工业制法用硫铁矿(主要成分为FeS2)还原氯酸钠制取二氧化氯,某研究小组在实验室设计如下装置制备ClO2的水溶液。

(1)三颈烧瓶中加入NaClO3溶液、浓H2SO4,通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。反应开始时烧瓶内发生反应的离子方程式如下,请配平该方程式:□ClO3- +□FeS2+□H+=□ClO2+□Fe3++□SO42-+□H2O
(2)装置D的作用是 。
(3)用上述反应完后的废液(除上述产物外,还有Al3+、Mg2+、H+、Cl-等)可制备摩尔盐,即(NH4)2Fe(SO4)2·6H2O。其操作流程如下:

回答下列问题:
①操作Ⅰ的名称为: 。
②试剂X是 ,写出发生的主要反应的离子方程式 。
③为测定(NH4)2Fe(SO4)2·6H2O晶体中铁的含量,某实验小组做了如下实验:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250mL溶液。取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,用0.01000mol/L KMnO4溶液滴定至Fe2+恰好全部氧化成Fe3+,同时,MnO4_被还原成Mn2+。测得消耗KMnO4溶液的平均体积为21.00mL。则该晶体中铁的质量分数为 。(保留4位有效数字)
(1)15ClO3- + FeS2+ 14H+= 15ClO2+ Fe3++2SO42-+7H2O (3分)
(2)检验ClO2是否吸收完全(2分)
(3)①过滤(2分) ②Fe(2分); 2Fe3++Fe=3Fe2+(2分);③11.76%(3分)
题目分析:(1)配平时,铁和硫元素是按照1﹕2进行的,总共失去十五摩尔的电子,而氯元素总共得到一摩尔的电子,因此在氯酸根离子前面乘以十五,然后按电荷守恒,和质量守恒来过行配来,就可以得到如下关系式:15ClO3- + FeS2+ 14H+= 15ClO2+ Fe3++2SO42-+7H2O (3分)
(2)因为二氧化氯(ClO2)是一种广谱、高效的杀菌消毒剂,其一定具有强烈的氧化性,如若没有被吸收完的话,进入到最后的D瓶中,可以使品红褪色,所以是用来检验ClO2是否吸收完全的(2分)
(3)第一步,是要用过量的铁将生成的三价铁离子还原为二价,因此①的操作是过滤(2分) ②Fe(2分); 2Fe3++Fe=3Fe2+(2分);
③假设铁离子的物质的量为xmol
MnO4_ ~ ~ ~ 5Fe2+
1mol 5mol
0.01000mol/L×21.00mL×10 x
解之得:x=1.05×10-2mol,则铁的质量分数为:
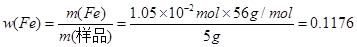 =11.76%
=11.76%
