问题
实验题
以工业碳酸钙(含有少量NaCl、AlCl3、FeCl3等杂质)生产氯化钙的主要流程如下。
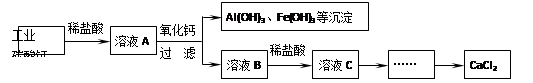
写出碳酸钙与稀盐酸反应和氧化钙与水的化学方程式为 、
。取少量溶液B于试管中,滴入紫色石蕊试液,溶液变
为 色,溶液B中含有的溶质为 和 (填化学式)。
答案
CaCO3+2HCl→CaCl2+H2O+CO2↑ CaO+H2O→Ca(OH)2 (2分)
蓝 CaCl2 Ca(OH)2 (3分)
本题考查的是物质的相互转化和制备,盐的化学性质,化学式和化学方程式的书写。根据所学知识可以知道碳酸钙可以和盐酸反应生成氯化钙:CaCO3+2HCl=CaCl2+H2O+CO2↑;氧化钙和水反应生成氢氧化钙:CaO+H2O= Ca(OH)2;碳酸钙与盐酸反应生成氯化钙,在溶液A中加入氧化钙,氧化钙和水反应生成氢氧化钙,故溶液B中含有的溶质是氯化钙和氢氧化钙,化学式为:CaCl2 和Ca(OH)2;碱溶液使紫色石蕊试液变蓝。
