已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)X、Y、Z、W四种元素的名称:Y______、W______
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为
______.
(3)由X、Y、Z所形成的离子化合物与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是______.
(4)由X、Y形成的化合物XY5属于______晶体,写出XY5和水的反应方程式______.
(1)Y的氢化物分子中有3个共价键,Y应为N元素,Z原子最外层电子数是次外层电子数的3倍,则Z为O元素,W原子的质子数等于Y、Z原子最外层电子数之和,则W为Na元素,X、W同主族,且原子序数最小,为H元素,故答案为:氮、钠;
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物分别是氨、氧化钠以及过氧化钠,其电子式分别为:
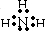
、

、
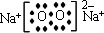
,故答案为:
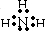
、

、
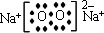
;
(3)由X、Y、Z所形成的离子化合物为NH4NO3,W的最高氧化物的水化物为NaOH,二者在加热条件反应生成氨气,
反应的离子方程式为NH4++OH-
NH3↑+H2O,故答案为:NH4++OH- △ .
NH3↑+H2O; △ .
(4)Y形成的化合物XY5属于离子晶体,为NH4H,含有-1价的H元素,具有强还原性,与水反应生成氢气,反应的化学方程式为NH4H+H2O═NH3•H2O+H2↑,
故答案为:离子;NH4H+H2O═NH3•H2O+H2↑.
