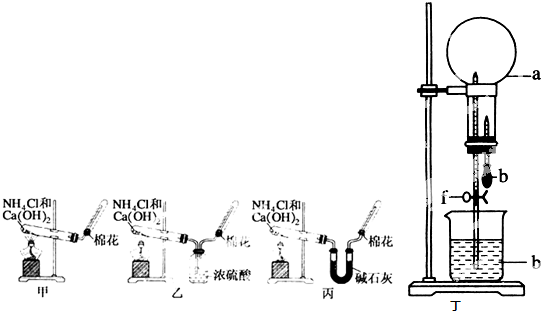
甲、乙、丙三位同学分别用如下甲、乙、丙三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气.请你参与探究,并回答下列问题:
(1)三位同学制取氨气的化学方程式为:______.
(2)三位同学都用向下排空气法收集氨气,而不用排水法,其原因是______
A.氨气难溶于水 B.氨气极易溶于水
C.氨气密度比空气大D.氨气密度比空气小
E.氨气密度比水大F.氨气密度比水小
(3)三位同学用上述装置制取氨气时,其中乙同学没有收集到氨气,收集不到氨气的主要原因是______(用化学方程式表示).
(4)检验氨气是否收集满的方法是______.
A.闻到有氨气逸出
B.棉花被气体冲出
C.用湿润的红色石蕊试纸在试管口检验,发现试纸变蓝
D.用湿润的蓝色石蕊试纸在试管口检验,发现试纸变红
(5)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的是______(填“甲”、“乙”或“丙”).
(6)要得到干燥的氨气可选用______作干燥剂.
A.碱石灰(CaO和NaOH的混合物)
B.浓硫酸
C.浓硝酸
D.氢氧化钠溶液
(7)用如图丁装置进行喷泉实验,烧瓶中已装满干燥氨气(标准状况),引发水向上喷的操作是______.
(1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑,△ .
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;△ .
(2)氨气易溶于水,不能用排水法收集,氨气密度比空气小,应用向下排空法收集,
故选:BD;
(3)氨气为碱性气体,通过盛有浓硫酸的洗气瓶时,与硫酸反应而被吸收,反应方程式为:2NH3+H2SO4=(NH4)2SO4,故答案为:2NH3+H2SO4=(NH4)2SO4;
(4)氨气为碱性气体,与水反应生成NH3•H2O,电离子出OH-离子,溶液呈碱性,检验时可用用蘸有浓盐酸的玻璃棒靠近试管口,如果产生白烟,则氨气已满,或用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满,故选:C;
(5)碳酸氢铵加热分解生成氨气、二氧化碳和水,其中可用碱石灰吸收二氧化碳和水,只有丙能做到,故答案为:丙;
(6)氨气是碱性气体所以能溶于酸,则氨气不能用酸干燥,氨气极易溶于水,所以氨气不能用水溶液干燥,故选A;
(7)打开止水夹,挤出胶头滴管中的水,氨气极易溶于水而使烧瓶内压强迅速减小,外界大气压不变,导致大气压大于烧瓶内压强,烧杯内水通过玻璃管进入烧瓶,从而形成喷泉,
故答案为:打开止水夹,挤出胶头滴管中的水.