硫酸铜晶体俗称“胆矾”,在无机化工及生产生活中有广泛的应用。某课外研究小组的同学用粗铜粉(含有碳等杂质)设计了两种制备胆矾的途径,并测定了其中结晶水的含量。设计的流程如下:
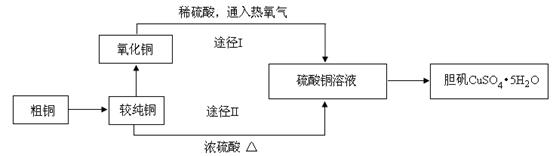
(1)“较纯铜”转化为氧化铜时,应将其置于 内进行灼烧(填写仪器名称)。“粗铜”表面的油脂可以用热碱溶液洗去,原因是 。若灼烧“粗铜”,获得的产物是混有少量铜的氧化铜。存在少量铜的可能原因是 。
a.灼烧过程中部分氧化铜被还原 b.该条件下铜无法被氧气氧化
c.氧化铜在加热过程中分解生成铜 d.灼烧不充分铜未被完全氧化
(2)通过途径I实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤是:酸溶、加热通氧气、过滤、 、冷却结晶、 、自然干燥。比较由粗制氧化铜制取胆矾的两种途径,途径Ⅰ有明显的两个优点:
① 。
② 。
(3)测定胆矾晶体里结晶水的含量时,若测定的相对误差大于零,则产生误差的原因可能是___________。
a.加热后容器未放入干燥器中冷却
b.最后两次加热后的质量相差较大
c.加热前称量时容器未完全干燥
d.加热过程中有少量溅失
(4)利用下图装置加热无水硫酸铜粉末直至完全分解,A的试管中剩余黑色粉末,用带火星的木条伸入集气瓶D,发现木条能复燃。反应前后各装置的质量见图下方的表格所示。
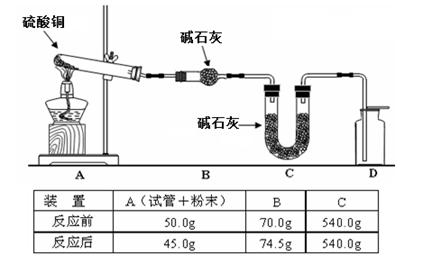
请通过计算,推断该实验条件下硫酸铜分解的化学方程式: 。
(1)坩埚;油脂在碱性条件下发生水解而除去 (2分,各1分)。 ad(2分,各1分)
(2)蒸发浓缩 过滤洗涤(2分,各1分)。①产生等量胆矾,途径I消耗硫酸少;②途径I不产生污染大气的气体(2分,各1分)
(3)cd(2分,各1分)
(4)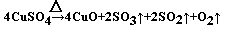 (2分,产物质正确1分,配平1分)
(2分,产物质正确1分,配平1分)
题目分析:(1)进行灼烧所需的温度较高应选择坩埚,“粗铜”表面的油脂可以用热碱溶液洗去,原因是油脂在碱性条件下发生水解而除去。若灼烧“粗铜”,获得的产物是混有少量铜的氧化铜。存在少量铜的可能原因是a.灼烧过程中部分氧化铜被还原 d.灼烧不充分铜未被完全氧化。
(2)过滤完后还要进行蒸发浓缩然后冷却结晶、过滤洗涤,最后再自然干燥。途径Ⅰ有明显的两个优点:①对照反应转化情况可知产生等量胆矾,途径I消耗硫酸少;②途径I不产生污染大气的气体。
(3)测定的相对误差大于零说明水的量较多或固体的质量较少,a.加热后容器未放入干燥器中冷却不一定产生误差;b.最后两次加热后的质量相差较大也可能会使水的质量减小; c.加热前称量时容器未完全干燥,会有水将会使水的量增多,正确;d.加热过程中有少量溅失,将会使剩下的固体质量减少,相当于水的量增多,正确;
(4)加热无水硫酸铜粉末直至完全分解,A的试管中剩余黑色粉末,用带火星的木条伸入集气瓶D,发现木条能复燃,说明有氧气生成。由记录的数据可得出生成酸性气体质量是4.5g,生成氧气是0.5g,生成固体物质45g,根据电子守恒,由生成氧气0.5g,失电子数(0.5/32)*4mol。得电子可能是生成了二氧化硫,即生成二氧化硫的量为:(0.5/32)*2mol,质量为2g,还有酸性气体应该是三氧化硫,质量为2.5g,物质的量为2.5/80mol,即物质的量之比:二氧化硫:三氧化硫:氧气=2:2:1,根据原子守恒可知生成黑色固体为氧化铜,化学方程式为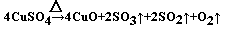 。
。
