实验室用N2、H2合成氨气,并用酚酞试液检验生成的氨气,用锌与盐酸反应制取氢气;用NaNO2饱和溶液和NH4Cl饱和溶液共热制取氮气: NaNO2+NH4Cl=NaCl+NH4NO2;NH4NO2 N2↑+2H2O。制取装置如图所示:
N2↑+2H2O。制取装置如图所示:
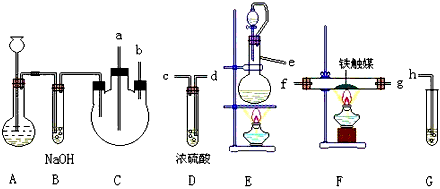
(1)装置A用于制取______________
(2)装置E中分液漏斗上方常用导管与园底烧瓶相通,作用是______________。装置E与装置C直接相连,连接时导管口连接方法为e接______________。
(3)装置C的另一接口与其他仪器装置相连接时,导管口的连接顺序为:另一接口_____接______,____接_____,______接______。
(4)装置D的作用为______________。装置F导出的气体的成分为______________。
(5)装置G内滴有酚酞的试液,用于检验氨气的生成,该装置中导管口能否插入液面以下__________(填“能”或“不能”),理由是_________________________。
(6)从充分利用原料的角度看,装置G应装双孔塞,此时另一接口应与________相连为佳。
(1)H2(或氢气)
(2)便于液体顺序流下;b
(3)a;d;c;f;g;h
(4)干燥N2、H2;NH3、H2、N2
(5)不能;氨气极易溶于水而发生倒吸
(6)d
