(13分)纳米碳酸钡是一种重要的无机化工产品,下图是某厂生产纳米碳酸钡的工艺流程。请回答下列问题:
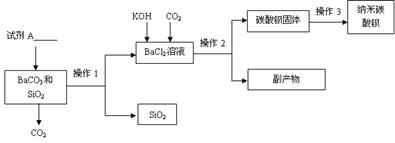
(1)试剂A的化学式 ,若在实验室中进行该实验,操作1和操作2的名称是 ,该实验中玻璃棒的作用 。
(2)操作3为洗涤、检验和 ,洗涤的作用是
,检验洗涤是否干净可选用试剂 (写化学式)。
(3)上述流程中可循环利用的物质是 ,该流程中的副产物可用作
。(写一种用途)
(4)分析该流程可得出SiO2部分性质,下列属于其物理性质 ,化学性质 。
A.不溶于水
B.可溶于水
C.不与盐酸反应
D.能与盐酸反应(5)某同学查阅资料得知,二氧化硅能与氢氧化钠溶液反应生成可溶性的硅酸钠(Na2SiO3),该反应的化学方程式 。根据此原理该同学设计出如下方案制备:取碳酸钡和二氧化硅混合物,滴加 (填“少量”或“过量”)的氢氧化钠溶液,过滤,洗涤,烘干得碳酸钡固体。
(13分)(1)HCl 过滤 引流
(2)烘干 除去沉淀表面可溶性杂质或残留滤渣表面滤液 AgNO3
(3)CO2 钾肥或钾盐
(4)A C
(5)2NaOH +SiO2══Na2 SiO3+ H2O 过量
(1)由氯化钡溶液可知试剂A中含有氯离子,没有新的离子产生只能是HCl,分离不溶性固体和液体混合物只有过滤,
(2)AgNO3与氯化钡和氢氧化钾会产生白色沉淀氯化银或氢氧化银
(3)盐酸和碳酸钡会产生二氧化碳,产生碳酸钡也用到二氧化碳,可循环利用的物质是二氧化碳,副产物中有钾离子可用作钾肥或钾盐
(4)物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质
(5)反应物是氢氧化钠和二氧化硅,生成物是硅酸钠和水,根据质量守恒定律书写化学方程式,因为二氧化硅不溶于水,只有过量滴加氢氧化钠溶液才能把二氧化硅全部反应,过滤后得到纯净的碳酸钡固体。
