问题
实验题
高纯氧化铁(α-Fe2O3)是现代电子工业的重要材料。实验室用硫铁矿烧渣(主要成分是Fe2O3、FeO、SiO2等)为原料制备高纯氧化铁的步骤如下:
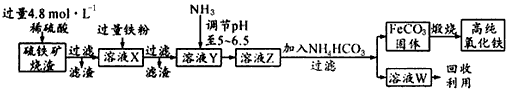
请回答下列问题:
(1)实验室用18.4 mol/L的浓硫酸配制250 mL 4 8 mol/L的硫酸溶液,所用的玻璃仪器除胶头滴管、量筒、烧杯、玻璃棒和酸式滴定管外,还需_________(填写仪器名称)。
(2)溶液X中加入铁粉后可能发生反应的离子方程式为______________________
(3)某同学选用下列装置来制备纯净干燥的氨气,请完成下列有关问题:
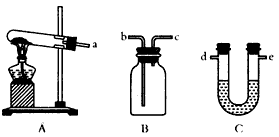
①装置A中可以选用下列试剂中的___________(填写序号字母);
a.(NH4)2SO4和生石灰 b.NH4Cl和Ca(OH)2固体 c.NH4HCO3固体 d.NH4Cl固体
②装置C中试剂最好选用_________(填写试剂名称);
③收集NH3时,气体应由_________(填写导管口代号)通入。
(4)写出氨水与NH4HCO3溶液反应的离子方程式__________________
答案
(1)250mL容量瓶
(2)2Fe3+ +Fe=3Fe2+、2H+ +Fe=Fe2+ +H2↑
(3)①bc;②碱石灰(其他合理答案也可);③c
(4)NH3·H2O+HCO3-=NH4++CO32-+H2O
