某同学用下列装置制备并检验Cl2的性质。
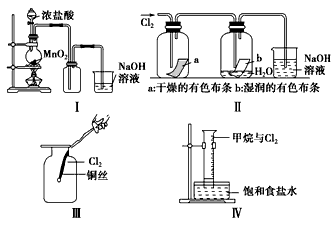
(1)Ⅰ图圆底烧瓶中反应的化学方程式为________________。
(2)Ⅱ图中退色的是A____(填“a”或“b”),Ⅱ图烧杯中发生反应的离子方程式是________________。
(3)将铜丝换成铁丝,做Ⅲ实验,结果也能点燃,你认为铁丝也能点燃的理由是A______(填选项字母)。
A.Fe与Cu都是金属元素 B.Fe的熔点比Cu高 C.Fe的密度比Cu小 D.Fe的金属性比Cu强
(4)将Ⅳ装置放置在光亮的地方(日光没有直接照射),一会儿后,观察到量筒壁上有油状液滴生成,饱和食盐水中有少量固体析出,量筒内黄绿色气体颜色变浅,量筒内液面上升等。
①油状液滴的成分可能是(写分子式) _____________。
②水槽用饱和食盐水而不用水的原因是__________________。
③饱和食盐水中有少量固体析出,其原因是__________________。
(5)将硫酸溶液滴入Ⅱ图实验后的烧杯中,至溶液显酸性,结果也有Cl2生成,其原因是(用离子反应方程式表示)__________________。
(1)MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)b;Cl2+2OH-===Cl-+ClO-+H2O
(3)D
(4)①CH2Cl2、CHCl3、CCl4;②降低Cl2在水中的溶解度,抑制Cl2和水的反应;③反应中有HCl生成,使溶液中的Cl-浓度增大,促使NaCl的溶解平衡向生成NaCl固体的方向移动
(5)Cl-+ClO-+2H+==Cl2↑+H2O
