问题
问答题
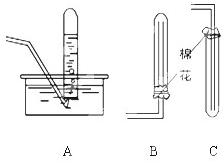
氨是重要的化工原料,实验室制取氨气的化学方程式为______,如图所示,A、B、C是气体收集装置,其中可用来收集氨气的是______.当两根分别蘸有浓氨水和浓盐酸的玻璃棒靠近时,会观察到的现象是______.在实验室,干燥氨时,通常是将制得的氨通过______,以除去其中的水蒸气;为检验氨气是否收集满,往往取______试纸置于试管口处,当颜色由______ 时,表明已经收集满氨气.
答案
实验室用氯化铵和氢氧化钙制取氨气,反应方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O, △ .
氨气极易溶于水,常温下,氨气不和空气反应,氨气的密度小于空气,所以氨气可以采用向下排空气法收集,故选B,
氨气和氯化氢反应生成固体氯化铵,所以会看到有白烟生成,氨气是碱性气体,所以在实验室,干燥氨气时通常用碱石灰,氨气能使湿润的红色石蕊试纸变为蓝色,
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;B;有白烟生成;碱石灰;湿润的红色石蕊;红色变为蓝色. △ .
