选做题,本题有A、B两题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容,请选择其中一题作答,并把所选题目对应字母后的方框涂黑.若两题都作答,将按A题评分.
A.可以由下列反应合成三聚氰胺:
CaO+3C
CaC2+CO↑ CaC2+N2 高温 .
CaCN2+C↑ CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺. 高温 .
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
______.CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和______(填化学式),由此可以推知CN22-离子的空间构型为______.
(2)尿素分子中C原子采取______杂化.尿素分子的结构简式是______,其中碳氧原子之间的共价键是______(填字母)
A.2个σ键 B.2个π键 C.1个σ键、1个π键
(3)三聚氰胺(
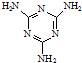
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
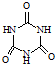
)后,三聚氰酸与三聚氰胺分子相互之间通过______结合,在肾脏内易形成结石.
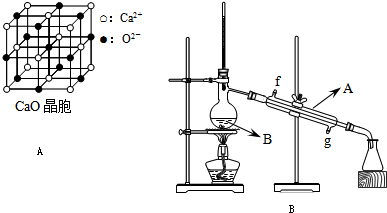
(4)CaO晶胞如图A所示,CaO晶体中Ca2+的配位数为______.CaO晶体和NaCl晶体的晶格能分别为:CaO 3401kJ/mol、NaCl 786kJ/mol.导致两者晶格能差异的主要原因是______.
B.实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的物理性质如下表.请回答有关问题.
| 化合物 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:______、______.
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是:______、______.
Ⅱ.乙酸正丁酯粗产品的制备
(1)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠洗涤,正确的操作步骤是______(填字母).
A.①②③④B.③①④②C.①④①③②D.④①③②③
(2)将酯层采用如图B所示装置蒸馏.
1.出图中仪器A的名称______.冷却水从______口进入(填字母).
2.②蒸馏收集乙酸正丁酯产品时,应将温度控制在______左右.
Ⅲ.计算产率
测量分水器内由乙酸与正丁醇反应生成的水体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率______.
A(1)与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子是锌,根据构造原理,基态的锌原子核外电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2;与CN22-互为等电子体的分子有N2O和CO2;等电子体具有相同的价电子数、原子总数,结构相似,二氧化碳分子是直线型,所以CN22-离子的空间构型是直线型.
故答案为:1s22s22p63s23p63d104s2或[Ar]3d104s2;CO2;直线型.
(2)CO(NH2)2分子中中心原子C原子上含有三个σ键一个π键,所以空间构型是平面三角形的,碳原子采取sp2杂化,尿素分子的结构简式是

,其中碳氧原子之间的共价键是1个σ键、1个π键
,故选C.
故答案为:sp2,

,C.
(3)三聚氰酸与三聚氰胺分子相互之间能形成氢键,所以是通过分子间氢键结合,在肾脏内易形成结石.
故答案为分子间氢键.
(4)以钙离子为中心,沿X、Y、Z三轴进行切割,结合图片知,钙离子的配位数是6;
晶格能大小与离子带电量成正比,CaO晶体中Ca 2+、O 2-的带电量大于NaCl晶体中Na+、Cl-的带电量,导致氯化钠的晶格能大于氧化钙的晶格能.
故答案为:6,CaO晶体中Ca 2+、O 2-的带电量大于NaCl晶体中Na+、Cl-的带电量.
BⅠ(1)醇在一定条件下能发生分子内或分子间脱水生成醚或烯烃,所以该条件下,正丁醇能发生分子间脱水形成醚CH3CH2CH2CH2OCH2CH2CH2CH3,也能形成分子内脱水生成正丁烯CH2=CHCH2CH3.
故答案为:CH3CH2CH2CH2OCH2CH2CH2CH3;CH2=CHCH2CH3.
(2)实验中为了提高乙酸正丁酯的产率,使反应向正反应方向移动,所以采取的措施是用分水器及时移走反应生成的水,减少生成物的浓度;使用过量醋酸,提高正丁醇的转化率.
故答案为:用分水器及时移走反应生成的水,减少生成物的浓度;使用过量醋酸,提高正丁醇的转化率.
Ⅱ.(1)因为正丁醇和乙酸都具有挥发性,所以制取的酯中含有正丁醇和乙酸,第一步水洗除去酯中的正丁醇和乙酸;
第二步用10%碳酸钠洗涤除去乙酸;
第三步用水洗涤除去碳酸钠溶液;
第四步用无水硫酸镁干燥除去水;
第五步蒸馏,制得较纯净的酯.
故选C.
(2)1起冷凝作用的仪器名称是冷凝管,为防止炸裂冷凝管,水应从下口进上口出.
2根据酯的温度知,温度应控制在126.1℃.
故答案为:冷凝管;下;126.1℃.
Ⅲ.正丁醇的质量=0.810 g/mL×11.5mL=9.315g;冰醋酸的质量=1.049g/mL×9.4mL=9.86g;
先根据方程式判断哪种物质过量,以不足量的为标准进行计算.
理论上9.315g正丁醇完全反应生成酯的质量为xg,生成1.8g水时同时生成酯的质量是yg.
乙酸和正丁醇的反应方程式为CH3COOH+CH3CH2CH2CH2OH
CH3COOCH2CH2CH2CH3+H2O浓硫酸 △
60g 74g 116g 18g
9.315g xg
yg 1.8g
所以x=14.6
y=11.6
乙酸正丁酯的产率=
×100%=79.4%.11.6g 14.6g
故答案为79.4%.
