第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
(1)Cr的核外电子排布式为______;
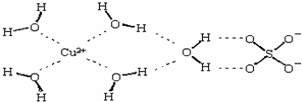
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:图中虚线表示的作用力为______;
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4•H2O晶体.在Cu(NH3)4SO4•H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是______,该原子团中心原子的杂化轨道类型是______;
(4)在一定条件下,Cu+比Cu2+稳定,请解释其原因:______
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是______,Ni(CO)4易溶于______.
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.
(1)Cr的原子序数为24,基态原子的电子排布式为1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1;
(2)Cu2+与O之间为配位键,H…O为氢键,故答案为:氢键、配位键;
(3)S与4个O形成共价键,则含有4个δ键,孤电子对数=
=0,应为sp3杂化,且为正四面体结构,6+2-2×4 2
故答案为:SO42-;sp3;
(4)Cu+基态离子的价电子排布为3d10,Cu2+基态离子的价电子排布为3d9,二者比较前者为半充满,为较稳定状态,
故答案为:Cu+基态离子的价电子排布为3d10,Cu2+基态离子的价电子排布为3d9,前者为半充满,所以Cu+比Cu2+稳定;
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,应为分子晶体,呈正四面体构型,应为非极性分子,易溶于非极性溶剂,
故答案为:分子晶体;BC.