四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃.装置A中放浓盐硫,B中放MnO2,二者用于制氯气,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热).请回答下列各问题.
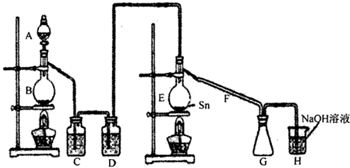
(1)图中气体发生和尾气处理装置不够完善,请你提出改进意见______.
利用改进后的正确装置进行实验,请回答下列问题:
(2)H中反应的离子方程式:______;E中反应的化学方程式:______.
(3)C、D中的试剂分别是______、______.
(4)仪器A、B的名称分别是______、______,F的作用是______.
(5)实验时应先点燃______处酒精灯,加热温度应大于______℃,待______即可停止加热.
(6)已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,那么四氯化锡水解的化学方程式为______.
(7)如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是______.
(1)发生装置中生成气体,压强增大,分液漏斗中的盐酸不能顺利加到圆底烧瓶中,应用导管将A的上口与B相连,以平衡分液漏斗与圆底烧瓶中的压强,
四氯化锡极易水解,G为收集四氯化锡装置,应在G、H之间增加干燥装置防止H中的水蒸气加入G装置,
故答案为:用导管将A的上口与B相连;在G、H之间增加干燥装置;
(2)H为吸收为反应的氯气,氯气与氢氧化钠反应生成氯化钠、次氯酸钠、水,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
由装置图可知,E中为金属锡跟干燥的氯气反应生成无水四氯化锡,反应方程式为:Sn+2Cl2
SnCl4, △ .
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;Sn+2Cl2
SnCl4; △ .
(3)四氯化锡极易水解,进入装置E的气体应干燥、纯净,装置C的作用为吸收挥发出的HCl,用饱和食盐水吸收HCl,装置D的作用为吸收水蒸气、干燥气体,用浓硫酸吸收干燥,
故答案为:饱和食盐水;浓硫酸;
(4)仪器A为分液漏斗,B为蒸馏烧瓶,F起导气、并冷凝四氯化锡蒸气,
故答案为:分液漏斗;蒸馏烧瓶;导气、冷凝;
(5)熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡,故应向加热E酒精灯,加热温度应大于金属锡的熔点,当锡融化后停止加热,
故答案为:E;231;锡融化;
(6)四氯化锡遇水强烈水解,由水解原理可知,应生成Sn(OH)4、HCl,产物之一是固态二氧化锡,说明Sn(OH)4分解生成SnO2与H2O,故四氯化锡水解生成SnO2、HCl,反应方程式为:SnCl4+2H2O=SnO2+4HCl,
故答案为:SnCl4+2H2O=SnO2+4HCl;
(7)四氯化锡遇水强烈水解生成SnO2、HCl,SnO2是固体颗粒,HCl结合空气中的水蒸气,出现白色烟雾,故答案为:出现白色烟雾.
