传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高.DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量溶液的pH等而在中和滴定的研究中应用越来越广泛深入.
(1)某学习小组利用DIS系统探究强碱和不同酸的中和反应,实验过程如下:
①分别配制0.1000mol/L的NaOH、HCl、CH3COOH溶液备用.
②用0.1000mol/L的NaOH溶液分别滴定10.00mL0.1000mol/L的HCl和CH3COOH溶液,连接数据采集器和pH传感器.
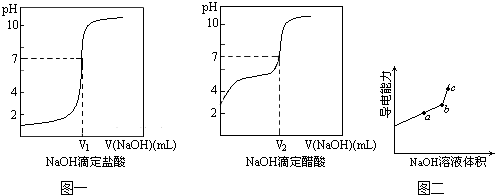
③由计算机绘制的滴定曲线如图一:
两曲线图起点不同的原因是______;两曲线图中V1______V2 (填“>”、“=”或“<”)
(2)另一个学习小组利用DIS系统测定某醋酸溶液的物质的量浓度,以测量溶液导电能力来判断滴定终点,实验步骤如下:
①用______(填仪器名称)量取20.00mL醋酸溶液样品,倒入洁净干燥锥形瓶中,连接好DIS系统.如果锥形瓶中含有少蒸馏水,是否会影响测量结果______(填“是”、“否”、“不能确定”).向锥形瓶中滴加0.1000mol/L的NaOH溶液,计算机屏幕上显示出溶液导电能力与加入NaOH溶液体积关系的曲线图(见图二).
②醋酸与NaOH溶液反应的离子方程式为______.
③图中b点时,溶液中各离子浓度大小的关系是______.
④若图中某一点pH等于8,则c(Na+)-c(CH3COO-)的精确值为______ mol/L.
(1)CH3COOH不完全电离,HCl完全电离,使0.1mol/L的CH3COOH溶液中c(H+)比同浓度的HCl溶液中c(H+)小,pH大;盐酸和NaOH反应生成氯化钠和水,氯化钠不水解,CH3COOH和NaOH反应生成醋酸钠和水,醋酸钠水解呈碱性,所以与等物质的量的盐酸、醋酸反应,反应后溶液呈中性,消耗的NaOH前者大于后者,故答案为:CH3COOH不完全电离,HCl完全电离,使0.1mol/L的CH3COOH溶液中c(H+)比同浓度的HCl溶液中c(H+)小,pH大;>;
(2)①用酸式滴定管量取20.00mL醋酸溶液样品;锥形瓶中含有少蒸馏水,待测液的物质的量不变,V(标准)不变,根据c(待测)=
,c(待测)不变,C(标准)×V(标准) V(待测)
故答案为:酸式滴定管;否;
②醋酸与NaOH溶液反应:CH3COOH+NaOH=CH3COONa+H2O,故答案为:CH3COOH+OH-=CH3COO-+H2O;
③图中b点,说明醋酸和NaOH恰好完全反应,醋酸钠水解,使得c(Na+)>c(CH3COO-),故答案为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
④c(H+)=10-8 mol/L,c(OH-)=
mol/L=10-6mol/L,根据电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),c(Na+)-c(CH3COO-)=c(OH--c(H+)=10-6mol/L-10-8 mol/L=9.9×10-7 mol/L,故答案为:9.9×10-7.10 -14 10 -8
