(7分)请根据下面的两个流程图回答问题,部分生成物已略去,未知物质均为初中化学常见物质。

(1)①反应的化学方程式为 。
(2)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水。则A的化学式为 ;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为 (写化学式);⑤反应的化学方程式为 。
(3)若A为金属单质,溶液甲为稀硫酸、溶液乙为硫酸铜溶液。则A的化学式为 ;向溶液D中加入过量的金属锌,发生反应的方程式为 。
(1)CH4 + H2O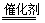 3H2 + CO
3H2 + CO
(2)CO2 Ca(OH)2、NaOH Na2CO3 + Ca(OH)2 CaCO3↓+ 2NaOH
(其它合理答案均可)
(3)Fe
Zn + H2SO4 ZnSO4 + H2↑ Zn + FeSO4 Fe + ZnSO4
Zn + CuSO4 ZnSO4 + Cu(2分)写出2个给1分,写出3个给2分。
题目分析:根据题意可知:
(1)①反应是CH4 和 H2O反应,其化学方程式为CH4 + H2O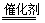 3H2 + CO;
3H2 + CO;
(2)若A为气体氧化物,与溶液甲和溶液乙反应均生成盐和水。则A是二氧化碳,它的化学式为CO2;取溶液D少量于试管中,加入碳酸钠溶液,有白色沉淀生成,则溶液D中溶质为氢氧化钙,化学式为Ca(OH)2;⑤的反应是前两步反应生成的碳酸钠和反应中剩余的氢氧化钙发生的反应,化学方程式为Na2CO3 + Ca(OH)2 CaCO3↓+ 2NaOH
(3)若A为金属单质,溶液甲为稀硫酸、溶液乙为硫酸铜溶液。则A是铁,其化学式为Fe;发生的反应有:Fe+ H2SO4 FeSO4 + H2↑;Fe + CuSO4 FeSO4 + Cu。溶液D为FeSO4溶液,向溶液D中加入过量的金属锌,发生反应的方程式为Zn + CuSO4 ZnSO4 + Cu。
点评:解答推断题的关键是找到突破口,并根据题中信息展开知识联想,题中的铁矿石是个很关键的信息点。
