(6分)某兴趣小组从铜器上取下绿色粉末,设计如下实验步骤进行探究铜绿的组成。
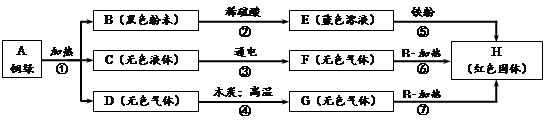
⑴写出:B物质的化学式 ;铜绿的组成元素 。
⑵我国古代有“曾青得铁则化为铜”的记载,这是现代湿法冶金的原理。这与上述实验方案中第 步骤(填数字编号)相似;化学方程式为 。
⑶写出第③步反应的化学方程式是 。
⑷在设计方案中有⑤⑥⑦三种冶炼铜的方法,通过比较请从资源、能源或环境等方面,说出其中一种方案所具有的优点: 。
(1)CuO;Cu、H、O、C;
(2)⑤;Fe+CuSO4=FeSO4+Cu (3) 2H2O  2H2↑+ O2↑
2H2↑+ O2↑
(4)用铁和硫酸铜反应的方法冶炼铜操作简单,不需加热(其他合理答案可给分)
题目分析:(1)根据题意可知,黑色粉末B和稀硫酸反应生成蓝色溶液E,则E中一定含有铜离子,则黑色粉末B为氧化铜,蓝色溶液E为硫酸铜溶液;硫酸铜溶液能和铁发生置换反应,生成铜(红色固体)和硫酸亚铁,由于H为红色固体,则H为铜;因为无色液体C在通电条件下能分解,根据所学化学知识可知,C为水;由于水电解生成氢气和氧气,则F为这两种气体中的一种,又根据图示,F和氧化铜加热能生成铜,说明F具有还原性,则F是氢气;根据图示,G也能与氧化铜加热反应,生成铜,说明G也具有还原性,且G是由D气体和木炭高温反应生成的,则G为一氧化碳,则D为二氧化碳,带入图示验证,正确。根据化学反应前后元素的种类不变可知,铜绿的组成元素为Cu、O、C、H。
(2)“曾青得铁则化为铜”是指铁与硫酸铜溶液发生反应,生成铜和硫酸亚铁,其反应的化学方程式是Fe+CuSO4=FeSO4+Cu,故与图示中的第⑤步相似。
(3)第③步的反应是水的电解,生成氢气和氧气,故其反应的化学方程式是2H2O 2H2↑+O2↑。
2H2↑+O2↑。
(4)实验方案评价的一般原则是:(1)理论正确;(2)操作可行;(3)经济合理;(4)推理严密;(5)保护环境。故一般不加热,操作简便,污染少,节约能源的方案都为较好的方案。
点评:解答本题的关键是根据明显现象找到突破点,即先要找准“题眼”,对于现象不明显的,要根据学过的知识先进行有针对性的猜想,然后沿着猜想进行推导,只要各步都满足,猜想就成立,如不满足,可再假设,再验证。
