有一瓶气体,可能是CO、CO2、H2O、H2中的一种或几种组成。为了分析该气体的成分,取适量该气体进行实验,实验方案设计如下:
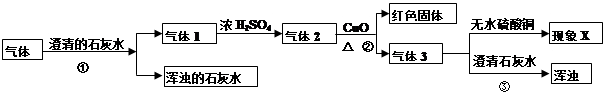
(查阅资料:白色无水硫酸铜粉末遇水变蓝色;浓H2SO4有吸水性,能干燥某些气体。)
(1)上述可能存在的气体中,易与血红蛋白结合的气体是______。
(2)实验中如果没有用浓H2SO4干燥气体1,对气体检验有无影响______。
(3)若现象X为“无水硫酸铜变蓝色”,结论是气体中 ;若现象X为“无水硫酸铜不变色”,结论是气体中 。
(4)②中一定发生的反应方程式是 。
(5)①③发生的反应相同,其反应的方程式是 。
(1)CO (2)有影响
(3)一定含有H2,一定不含H2(4)CuO + CO Cu + CO2
Cu + CO2
(5)CO2 + Ca(OH)2 ="=" CaCO3↓ + H2O
题目分析:根据几种气体的性质分析。
(1)一氧化碳有毒,它能与血液中的血红蛋白结合,从而导致体内组织器官严重缺氧而死亡。
(2)有影响,如果没有用浓H2SO4干燥气体1,那么气体2、3中都会含有水,则现象X一定是“无水硫酸铜变蓝色”,但不能说明该水是实验过程中带入的水,还是氢气与氧化铜反应生成的水,也就无法证明氢气的存在。
(3)由于气体1通过了浓硫酸,故气体2中肯定没有水,若现象X中“无水硫酸铜变蓝色”,说明气体3中含有水,则说明与CuO反应的混合气体中肯定有含有氢气;若现象X中“无水硫酸铜不变色”,说明气体3中不含有水,则与CuO反应的混合气体中肯定不含有氢气。
(4)由于气体3通入澄清的石灰水后,“澄清的石灰水变浑浊”,说明气体3中一定含有CO2,而之前的CO2已被除去,所以说明与CuO反应的混合气体中肯定有CO,故反应②中一定发生的反应方程式是CuO+CO Cu+CO2。
Cu+CO2。
(5)能使澄清石灰水变浑浊的原因是二氧化碳与氢氧化钙溶液发生反应生成不溶于水的碳酸钙沉淀,故其反应方程式为CO2 +Ca(OH)2=CaCO3↓+H2O。
点评:解答本题的关键是,熟记常见气体的检验与除杂方法及理论依据,以及氧气、氢气、二氧化碳、一氧化碳等气体的相关性质。

 特征的描述,哪项是错误的()
特征的描述,哪项是错误的()