分析下图所示实验回答问题(共4分)
甲乙两个瓶中都装有澄清的石灰水。在吸入气体时,左手捏紧橡皮管,右手松开。再呼出气体时,右手捏紧橡皮管,左手松开。
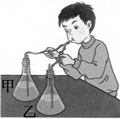
⑴一段时间后 瓶中的石灰水明显变浑浊。
说明呼出的气体中含有较多的 。
⑵发生气体交换的场所是 。
⑶若大气中,该气体的浓度过度增加,会引起 ( )
A.温室效应
B.酸雨
C.臭氧层破坏
D.大气污染
(4分) ⑴乙 二氧化碳 ⑵肺 ⑶A
分析:此题是一道实验分析题.通过实验来验证人体呼出的气体与吸入的气体进行比较,呼出的气体含有较多的二氧化碳.本实验中利用到二氧化碳能使澄清的石灰水变混浊这个特性来验证二氧化碳.解答此题的难点是,正确地理解甲、乙两装置的进气与出气设计.
解答:解:(1)在吸入气体时,左手捏紧橡皮管,右手松开,气体从甲瓶吸入因此甲装置就为吸气口.再呼出气体时,右手捏紧橡皮管,左手松开,呼出气体进入乙瓶,因此瓶是吹气用的.吸入气体含有的二氧化碳较少,没有使甲瓶澄清的石灰水变混浊,但进入人体后,在肺部毛细血管发生气体交换,空气中的氧气根据气体的扩散作用原理,扩散到毛细血管的血液中,毛细血管血液中的二氧化碳扩散到肺泡中,呼出体外,所以人呼出的气体含有的二氧化碳较多,故乙瓶的石灰水会变混浊.
(2)肺由许多肺泡构成,外面包绕着丰富的毛细血管和弹性纤维,肺泡的壁和毛细血管壁都很薄,只有一层上皮细胞构成,这些特点都有利于气体交换,因此肺是气体交换的主要场所,是呼吸系统的主要器官.(3)二氧化碳气体具有吸热和隔热的功能,二氧化碳在大气中增多的结果是形成一种无形的玻璃罩,使太阳辐射到地球上的热量无法向外层空间发散,其结果是地球表面变热起来.因此,二氧化碳的浓度过度增加,会引起温室效应,二氧化碳也被称为温室气体.
故答案为:
(1)乙;二氧化碳;
(2)肺;
(3)A.
点评:此题是一道实验操作题,如何进行实验,需要做题者认真思考后才能知道.所以做此题的突破口,首先从如何操作该实验装置入手