问题
问答题
在标准状况下,将224.L HCl气体溶于635mL(ρ=1.00g·cm-3)的水中,所得盐酸的密度为1.20g·cm-3。试求:
标准状况下,取这种盐酸100mL与足量的NaHCO3溶液反应后,放出多少升气体气体干燥后,通过盛有足量Na2O2固体的容器,充分反应后,容器内固体增重多少克
答案
参考答案:
9L 33.6g
解析:
(1)n(HCl)=224L/22.4L·mol-1=10.0mol
m(HCl溶液)=635g+10.0mol×36.5g·mol-1=1000g
c(HCl)= =" 12.0 " mol · L-1
=" 12.0 " mol · L-1
(2)n(HCI)=c·V=0.1L×12.0mol·L-1=1.20mool,
故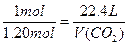
1mol 22.4L
1.20mol V(CO2)
V(CO2)=22.4L×1.20mol÷1mol=26.9L
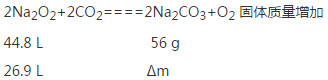
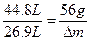 Δm="33.6" g
Δm="33.6" g
该盐酸的物质的量浓度为12.0 mol·L-1;放出的气体的体积为26.9 L;容器内固体增重33.6 g。
