(16)某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下:

(1)测定硝酸的物质的量
反应结束后,从下图B装置中所得100mL溶液中取出25.00mL溶液,用0.1mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如右上图所示。在B容器中生成硝酸的物质的量为 mol。
(2)测定NO的体积
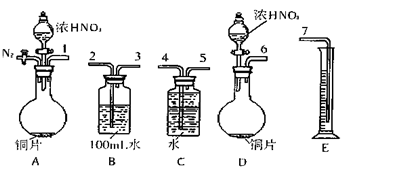
①从上图所示的装置中,你认为应选用 装置进行Cu与浓硝酸反应实验,选用的理由是 。
②选用上图所示仪器组合一套可用来完成实验并测定生成NO体积的装置,其合理的连接顺序是(填各导管口编号) 。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置
(“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析:若实验测得NO的体积为112.0mL(已折算到标准状况),则Cu与浓硝酸反应的过程中 (填“有”或“没有”)NO产生,作此判断的依据是 。
(4)实验前,用托盘天平称取的铜片至少应为 g。
(1)0.008(2分)
(2)A(2分,因为A装置可以通N2装装置中的空气排尽,防止反应生成的NO被装置内空气中O2氧化(2分)
②123547(2分,若只填出“1547”给1分) ③升高(2分)
(3)有(2分)
因为NO2与水反应生成的NO的体积小于收集到的NO的体积(89.6mL<112.0mL)(2分)
(4)0.5(2分)
(1)NaOH+HNO3=NaNO3+H2O
1 1
则:c(NaOH)V(NaOH)=n(HNO3),带入数据,得:
n(HNO3)=4×0.1mol·L-1×(20.40-0.40)×10-3L=0.008mol
(2) ②A中生成的气体可能有NO、NO2,通过B(3 NO2+H2O=2HNO3+NO)将NO2转化为NO,再通过C排水到E中,E中测得水的体积即为NO体积;
③若量筒中水的液面比集气瓶的液面要低,说明装置内气压小于外界气压,所以应将量筒的位置升高,以保证量筒中的液面与集气瓶中的液面持平;
(3)3 NO2+H2O=2HNO3+NO,由(1)知:n(HNO3)= 0.008mol
2 1
0.008mol 0.004mol
V(NO)= 0.004mol×22.4mol.L-1=89.6mL
即:NO2与水反应生成的NO的体积小于收集到的NO的体积(89.6mL<112.0mL)
(4) (4)由(3),得:n(NO2)=0.012mol,
反应中生成的n(NO)=(0.112-0.0896)L/22.4L·mol-1=0.001mol
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(浓)=3Cu(NO3)2+2NO↑+4H2O
1 2 3 2
0.006mol 0.012mol 0.0015mol 0.001mol
则n(Cu)= 0.006mol +0.0015mol="0.0075" mol,
所以:m(Cu)=" 0.0075" mol×64g·mol-1=0.48g,≈0.5g
