问题
选择题
含a molCu、b molAg的金属混合物与含c molHNO3的某浓度的硝酸恰好完全反应,生成的气体只有m molNO2和n molNO,下列式子成立的是( )
A.c=2a+b+m+n
B.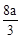 +2b="c"
+2b="c"
C. c=2m+2n
D.2a+b=m-3n
答案
答案:A
生成m molNO2和n molNO,则在反应中转移电子的物质的量是(m+3n)mol。而金属失去的电子是(2a+b)mol,所以根据得失电子守恒可知,m+3n=2a+b。a molCu、b molAg可以生成amolCu(NO3)2、bmolAgNO3,所以根据氮原子守恒可知2a+b+m+n=c。由此选项A正确,答案选A。

