(共10分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,反应方程式为2NH3+3CuO N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
N2+3H2O+3Cu,用示意图中的装置可以实现该反应。回答下列问题:
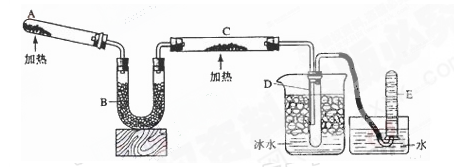
(1)A中发生反应的化学方程式是 。检验氨气通常采用的方法及现象是_________ ______, 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时C中观察到的现象是 ,该反应中氨的作用是_______剂。
(4)若要检验反应生成的水,可将试管D及烧杯部分改成两个相连的干燥管,第一个干燥管X内装有_____________,现象是___________________;第二个干燥管Y内装有碱石灰,作用是____________________________。
(1)2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O (1分)
2NH3↑+CaCl2+2H2O (1分)
用湿润的红色石蕊试纸(1分),试纸变蓝(1分)
(2)碱石灰,(1分)除去氨水中的水蒸汽(1分)
(3)黑色固体逐渐变成红色(1分),还原(1分)
(4)无水硫酸铜(1分),变蓝(1分)
防止E中的水蒸汽进入干燥管x,影响水的检验。(1分)
(1)A中是制取氨气的,所以方程式为2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O。氨气溶于水显碱性,和氯化氢反应冒白烟,据此可以检验。
2NH3↑+CaCl2+2H2O。氨气溶于水显碱性,和氯化氢反应冒白烟,据此可以检验。
(2)和氧化铜反应的氨气应该是干燥的,所以B中用碱石灰除去氨气中的水蒸气。
(3)氨气具有还原性,在加热的条件下,能还原氧化铜,生成铜、氮气和水,所以现象是黑色固体逐渐变成红色。
(4)检验水蒸气常用无水硫酸铜,遇水即变成蓝色。用于装置E中水蒸气可能进入干燥管。影响水的检验,所以作用就是防止E中的水蒸汽进入干燥管x,影响水的检验。
