(14分)某课外兴趣小组对双氧水(H2O2水溶液)做了如下实验探究。
(1)将质量相同但聚集状态不同的MnO2分别加入5mL 5%的双氧水中,并用带火星的木条试之。测定结果如下:
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,使木条复燃 | 3.5分钟 |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30分钟 |
②实验结果说明催化剂作用的大小与 有关。
(2)取三份含有等量H2O2,但质量分数不同的双氧水,分别向其中加入1克MnO2粉末。测定结果如下:
| 双氧水体积 | 操作情况 | 反应完成所需的时间 | 收集到气体体积 | 反应后液体温度 |
| a1%的150mL | 11分钟 | 539mL | 24℃ | |
| a2%的15mL | 混合不振荡 | 1分20秒 | 553mL | 56℃ |
| a3%的7.5mL | 9秒 | 562mL | 67℃ |
①反应完成所需的时间不同的原因 。
②反应后液体温度不同的原因 。
③收集到气体体积不同的原因 。
(3)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的双氧水,红色褪去。
①已知双氧水显弱酸性,试写出H2O2的电离方程式: 。
②小组讨论红色褪去的原因时,甲同学认为是双氧水显酸性所致;乙同学认为是双氧水有较强氧化性所致。请你设计一个简单实验来说明是甲对还是乙对。(简要文字说明)
(每空2分,共14分)
(1)①
②催化剂的表面积(聚集状态)
(2)①溶液质量分数不同,液体温度不同
②反应放热相同,但液体的量不同
③液体的量不同,液体温度不同(影响气体在溶液中的溶解量)
(3)①H2O2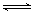 HO2-+H+(H2O2
HO2-+H+(H2O2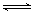 HOO-+H+)
HOO-+H+)
②在褪色溶液中再逐滴加入NaOH溶液,若红色恢复说明甲对,若红色不恢得则说明乙对
(1)①双氧水在催化剂的作用下,分解生成氧气,反应的方程式是2H2O2 2H2O+O2↑。
2H2O+O2↑。
②根据反应完成所需的时间课判断,催化剂作用的大小与催化剂的表面积(聚集状态)有关系。
(2)①由于溶液的质量分数不同,同时溶液的温度不同,从而导致反应速率不同,所以反应完成所需的时间不同。
②由于双氧水的质量相同,所以反应放出热量相同,但液体的量不同,所以溶液的温度是不同的。
③由于液体的量不同,且液体温度不同,从而影响气体在溶液中的溶解量,所以收集到的氧气是不同的。
(3)①双氧水可以看作是二元弱酸,电离是分步的,即H2O2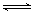 HO2-+H+(H2O2
HO2-+H+(H2O2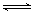 HOO-+H+)。
HOO-+H+)。
②如果是双氧水有较强氧化性所致,则再加入氢氧化钠溶液,是不能显红色的,加粗可以鉴别,即在褪色溶液中再逐滴加入NaOH溶液,若红色恢复说明甲对,若红色不恢得则说明乙对。
