(6分)成都市近年来常常发生“毒奶粉”事件。劣质奶粉制造商为牟取暴利,大大降低了奶粉中蛋白质的含量,导致食用这种奶粉的众多婴幼儿严重营养不良乃至死亡。
为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化为氨气(化学式为NH3),再用稀硫酸吸收氨气,反应的化学方程式为:2 NH3+H2SO4= (NH4)2 SO4
现取该奶粉样品100g,用“盖尔达法”分解其中的蛋白质,产生的氨气用7.5g溶质质量分数为19.6%的稀硫酸恰好完全吸收。
计算并回答下列问题:
(1)产生氨气的质量是多少?(计算结果精确到0.01,下同)
(2)含氮元素的质量多少?
(3)该奶粉中氮的含量是否达到了国家规定的标准。(奶粉中蛋白质的含量国家标准为:每100g婴幼儿奶粉中含12g~25g。蛋白质含氮元素的质量分数为16%)
(1)0.51g (2)0.42g (3)蛋白质的质量为2.63g,没有达到了国家规定的标准
考查根据方程式的有关计算。
(1)硫酸的质量是7.5g×19.6%=1.47g
2 NH3+H2SO4= (NH4)2 SO4
2×17 98
m 1.47g
所以m=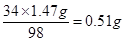
(2)含氮元素的质量是
(3)0.42g氮元素相当于蛋白质的质量是0.42g÷0.16=2.63g<12g
所以该奶粉中氮的含量没有达到了国家规定的标准。
